La maitrise du feu (du latin focus : feu, foyer, âtre) est à l’origine des plus remarquables acquisitions qui jalonnent la très longue évolution de l’humanité depuis des centaines de milliers d’années. Ses multiples usages balisent un cheminement qui passe par l’empreinte culturelle des civilisations, des croyances, des mythes associés traversant les âges. Quelles en ont été les grandes étapes ? En quoi consiste la combustion et que sait-on de ses différentes formes ? Quelles sont ses caractéristiques lors de la combustion du bois ? Ses usages massifs ne deviennent-ils pas problématiques pour la pérennité de la vie sur terre ?
1. Les grandes étapes de la combustion d’origine anthropique
La combustion de la matière combustible remonte à la nuit des temps, depuis la création de la terre, qui elle-même était à l’origine une boule de feu. Elle peut être produite de manière naturelle, comme les feux de forêts occasionnés par la foudre ou les volcans déversant leur lave incandescente sur la végétation. Elle est aussi entrée dans l’histoire des hommes avec la maîtrise du feu (Lire : Une brève histoire de l’énergie).
1.1. La maîtrise du feu

Longtemps après avoir taillé dans la pierre les premiers outils datant de – 2.5 millions d’années, les hommes ont définitivement quitté le stade animal en domestiquant une énergie naturelle et redoutable, le feu. Au tout début, le combustible utilisé était la matière végétale (herbes et bois) issue de l’environnement des premiers hommes (Figures 1 et 2). Leur découverte du feu remonterait à environ 450 000 ans, bien qu’une étude de chercheurs Israéliens considère qu’il faudrait pratiquement doubler cette datation, plutôt autour de 790 000 ans. Un site au nord d’Israël (Gesher Benot Ya’aqov) pourrait contenir la première trace connue de feu domestiqué par l’homo-erectus : un petit nombre d’objets brûlés (graines, bois) et de silex disposés de manière volontaire laissent supposer la présence de feux allumés et non naturels. Gesher Benot Ya’aqov est situé au carrefour des mouvements migratoires entre l’Afrique et le reste du monde. (Lire : Une brève histoire de l’énergie).
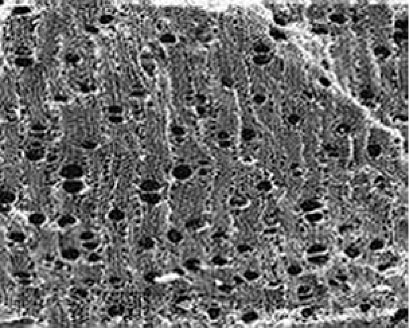
Qu’elle que soit la date, l’homme n’a cessé d’utiliser le feu pour ses différentes activités : cuire sa nourriture, se chauffer et se protéger des bêtes, mais aussi produire des feux de brousse et de forêt pour gagner des espaces. À suivi l’utilisation du feu dans les premiers fours à bois utilisés pour cuire le pain et transformer les métaux. L’âge du bronze puis du fer va être une grande épopée pour progressivement fabriquer des objets, des outils, instruments de la vie courante améliorant le confort de vie. L’artisanat se développe pour rendre accessible les produits de cette transformation au plus grand nombre à l’instar des maîtres de forges du Moyen-Âge (Lire : La consommation mondiale d’énergie avant l’ère industrielle).
Dans les manufactures qui se développent à partir du 17ème siècle, le feu est largement utilisé pour la transformation des métaux indispensable à la construction de ponts et d’édifices divers, de nouveaux moyens de transport tels que chemins de fer et bateaux, tous gros consommateurs d’acier et autres métaux dont la production exige de la combustion. Pour se déplacer, l’homme en utilise également sous forme d’oxydo-réduction dans les moteurs thermiques des trains, voitures, avions ou navires. Pour chauffer les bâtiments de grandes quantités de combustible d’origines fossiles, charbon, pétrole, gaz, sans oublier le bois, doivent être mobilisées.
1.2. Les mythes et le mysticisme associés au feu
Le feu a construit l’homo-sapiens avec les mythes et le mysticisme qui traversent les âges et les civilisations. Dans la philosophie chinoise, il fait partie des cinq éléments avec le métal, l’eau, le bois et la terre. Chez les alchimistes occidentaux, il fait aussi partie des quatre éléments inertes de base composant chaque matière avec l’eau, l’air et la terre selon l’enseignement d’Aristote.

Le feu est naturellement associé au soleil, source de chaleur et de lumière : Hélios dans la mythologie grecque et romaine ; la vénération du feu bleu Xiuhtecuhtli-Xoxoauhqui par les Aztèques. Le feu fascine avec les démons de la terre, que sont les volcans, ou sous la forme du feu de la forge d’Héphaïstos/Vulcain, dieu du feu et des forges (Figure 3). Il est également associé à différents cultes et rites ancestraux tels que le feu de la Saint Jean. Au Moyen-Âge, il est utilisé comme instrument de justice (bûcher de l’inquisition), tout en contribuant à la légende des templiers avec les maîtres de forges. Il est aussi symbole de purification, sous la forme du bûcher pour la crémation dans la culture indienne.
Dans les pays d’Afrique, d’Asie, d’Amérique latine où le développement n’a pas apporté partout le confort de vie de l’Occident, le feu reste l’élément essentiel de survie de la cellule familiale, pour se chauffer et faire cuire les aliments. Il continue aussi d’être utilisé dans les campagnes pour entretenir les terrains par l’écobuage, bien que, dans nombre de pays, cette pratique fasse l’objet d’une réglementation stricte, compte tenu des risques d’incendies non maitrisés, en particulier dans les périodes de sécheresses.
Au 21ème siècle, le feu reste très présent dans le monde moderne. Il est installé au cœur de la maison, symbole du foyer (focus), soit pour chauffer et produire des thermies, soit pour le confort ou pour l’agrément intérieur des maisons. La fascination de cette transformation de la matière est bien exprimée par les buches de bois qui se consument dans la cheminée et par les flammes qui ramènent consciemment ou inconsciemment sans doute aux racines primitives. Le poids culturel qu’il représente au travers des différentes civilisations est encré dans la mémoire reptilienne de l’homo sapiens. Les progrès techniques rappellent peut être aussi qu’il faut sauvegarder l’instinct de conservation qui anime l’homme depuis qu’il a découvert et maitrisé le feu.
1.3. La matière et le feu

Mais qu’est au juste le feu ? Quelles sont ses relations avec la matière ? Dès l’antiquité, les philosophes grecs croyaient qu’elle était constituée de quatre éléments: la terre, l’eau, le feu et l’air. Cette croyance trouvait une explication dans l’observation de la combustion d’un morceau de bois qui produisait de la fumée (air) de la vapeur (eau) et de la cendre (terre). Cette théorie dite phlogistique (phlogistos signifie inflammable) résultait des observations de philosophes tels que Thalès et Empédocle (Figure 4).

La théorie phlogistique est reprise et développée à la fin du 17ème siècle par Johann Joachim Becher médecin chimiste allemand, puis, jusqu’au 18ème siècle, les scientifiques admettent les conclusions de l’Allemand Georg Ernst Stahl : le feu, sous la forme du phlogistique, est contenu dans la matière elle-même, la combustion n’en étant que la libération. Cette théorie est d’autant mieux acceptée qu’elle correspond à un retour aux idées des philosophes grecs, notamment à la vision élémentaire sur l’univers et ses quatre éléments : eau, terre, air et feu. Il faudra attendre Antoine Laurent de Lavoisier pour découvrir les principes de la combustion par l’oxygène en 1775 qui rendent caduques la théorie phlogistique (Figure 5).
Depuis la connaissance des principes physico-chimiques de la combustion, l’homme n’a cessé de perfectionner les systèmes de conversion des sources d’énergie par le feu pour en améliorer l’efficience dans les différents usages (Figure 6). Il se heurte cependant aux limites des rendements qui, au niveau de la conversion des sources d’énergie, ne sont pas toujours très élevés, d’où des pertes liées aux principes même de cette conversion, en particulier lorsqu’elle porte sur des combustibles d’origines fossiles.

1.4. Vue d’ensemble sur le progrès des connaissances
L’histoire du feu, ou des combustions sous toutes leurs formes, s’est extraordinairement accélérée au cours d’une période de temps très courte (Figure 7).
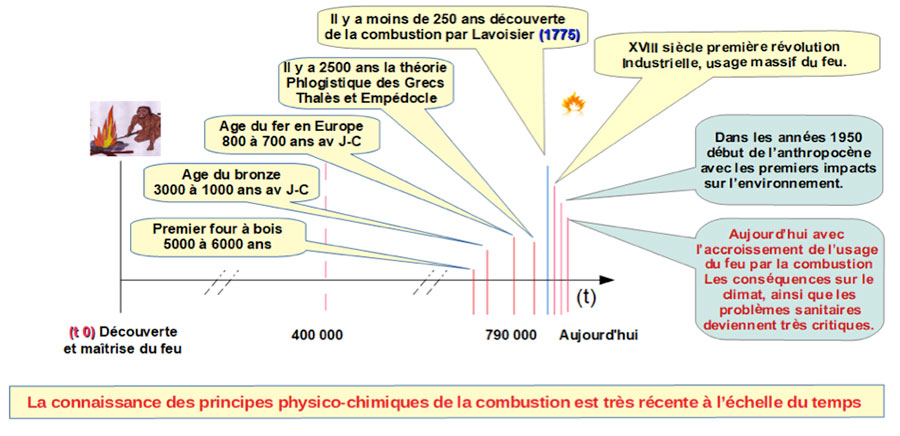
Cette accélération de l’histoire du feu peut être illustrée par la suite des inventions et des perfectionnements techniques observée depuis le 18ème siècle (Tableau 1).
Tableau 1 : Progrès des connaissances
| Chronologie | Découvertes et inventions | Datation |
| Homo erectus | Découverte de la maitrise du feu | 450 000 ans à 790 000 ans ? |
| Civilisation Egyptienne et Mésopotamienne | Premier four à bois pour la cuisson du pain | 5000 – 6000 ans |
| Protohistoire | Âge du bronze | 3000 à 1000 av JC |
| Dépend de l’aire culturelle et géographique | Âge du fer | 800 à 700 av JC |
| Grecs | Théorie phlogistique du feu
par les philosophes grecs |
500 av JC |
| Moyen âge | Les premiers maitres de forge | 5 à 15 siècle |
| Denis Papin | Première chaudière (autocuiseur) | 1679 |
| Pierre-Clément Grignon
(Maitre de forges) |
Première attestation du terme sidérotechnie qui deviendra sidérurgie | 1761 |
| James Watt | Chambre à vapeur (prémisse du moteur) | 1769 |
| Nicolas Joseph Cugnot | Premier véhicule automobile terrestre
actionné par la vapeur |
1770 |
| Antoine Laurent de Lavoisier | Découverte du principe de combustion par l’oxygène | 1775 |
| Claude François / Jouffroy d’Abbans | Premier bateau à vapeur | 1776 |
| Première révolution industrielle
|
Machine à vapeur, sidérurgie au coke | Fin 18 au 19 |
| Richard Trevithick | Première locomotive à vapeur | 1804 |
| Etienne Lenoir | Premièr moteur à combustion interne
(2 temps) |
1860 |
| Clément Ader | Premier avion | 1890 |
| Deuxième révolution industrielle
|
Carburants et produits dérivés du pétrole | 1900 |
| Edmond Fouché | Premier chalumeau
soudeur oxyacétylénique |
1902 |
| Hermann Oberth | Première fusée | 1935 |
| Anthropocène
(impact des activités humaines sur l’environnement) |
Le terme d’anthropocène a été popularisé à la fin du 20ème siècle par le météorologue et chimiste de l’atmosphère Paul Joseph Crutzen, prix Nobel de chimie en 1995, et par Eugéne Stoemer biologiste, pour désigner une nouvelle époque géologique. | À partir des années 1950 |
| Source : Auteur | ||
2. Qu’est-ce que la combustion ?
Par sa flamme, le feu est la manifestation la plus visible du phénomène qu’est la combustion. Mais qu’est-ce que la combustion ? Pour produire du feu, il faut créer une réaction chimique de combustion qui est la résultante d’une oxydo-réduction. Il s’agit d’une composante majeure de la chimie à haute température qui implique principalement des réactions radicalaires à savoir la combinaison de trois éléments, le fameux triangle du feu (Figure 8) :

- le carburant : solide, liquide, gazeux, (bois, charbon, pétrole, gaz méthane ou autres) ;
- le comburant : l’air, plus précisément le dioxyde d’oxygène O2 un composé de l’air ;
- l’énergie d’activation : l’élément déclencheur du processus de la combustion, ce qu’est, par exemple, l’allumette que l’on craque sous une feuille de papier.
Sachant qu’oxydation signifie combinaison avec l’oxygène, dans une oxydo-réduction :
- le combustible est le corps qui est oxydé durant la combustion ; c’est un réducteur, il perd des électrons,
- le comburant est le corps qui est réduit ; c’est un oxydant, il gagne des électrons.
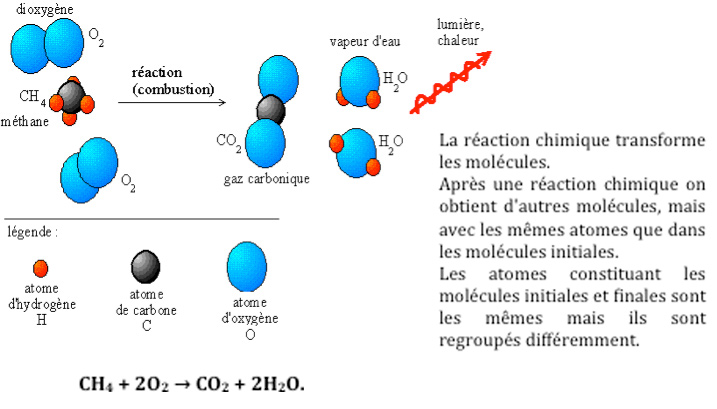
Le réducteur s’oxyde (réaction d’oxydation), l’oxydant se réduit (réaction de réduction). L’oxydoréduction se compose donc de deux demi-réactions : une oxydation et une réduction. L’oxydo-réduction produit de l’énergie sous forme de chaleur (exothermie). Si l’énergie produite par la combustion (oxydo-réduction) est supérieure ou égale à l’énergie d’activation la combustion s’auto entretien (Figure 9).
Il existe différents types de combustion, mais tous traduisent toujours un changement d’état moléculaire de la matière, à savoir une transformation moléculaire de la matière par la réaction chimique d’oxydoréduction. La combustion peut être très lente, c’est le cas de la rouille, ou extrêmement rapide, ce qui est le cas de l’explosion des gaz dans la chambre de combustion d’un moteur thermique, type automobile (Figure 10).
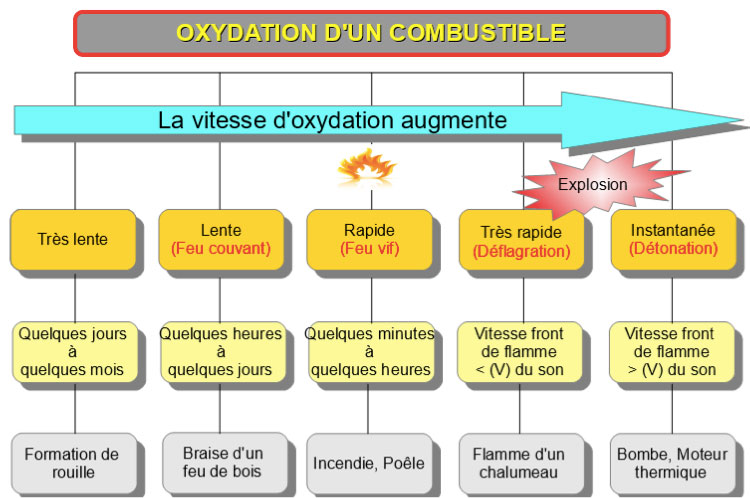
Dans un système thermodynamique, le niveau de l’énergie d’activation qui permet de changer d’état, de passer d’un état initial à un état final, se caractérise par l’enthalpie en physique, la fonction enthalpie étant une quantité reliée à l’énergie d’un système thermodynamique. Elle comprend l’énergie interne du système, à laquelle est ajouté le produit de la pression par le volume. L’enthalpie est un potentiel thermodynamique. Il s’agit d’une fonction d’état qui est une grandeur extensive, élément important d’un système thermodynamique (Lire : La thermodynamique : les lois et La thermodynamique : énergie et entropie).
C’est le scientifique néerlandais Heike Kamerlingh Onnes, prix Nobel de physique en 1913, qui aurait, le premier, introduit le concept. L’enthalpie se note H et, dans le système international, se mesure en joule (J). Elle est définie par la relation suivante :
H = U + PV
où U représente l’énergie interne,
P, la pression,
et V, le volume.
En d’autres termes, l’enthalpie représente l’énergie totale d’un système thermodynamique à savoir son énergie interne (U), c’est-à-dire l’énergie nécessaire à la création du système, plus le travail de détente (PV), qui correspond au travail que le système doit fournir contre la pression pour occuper son volume.
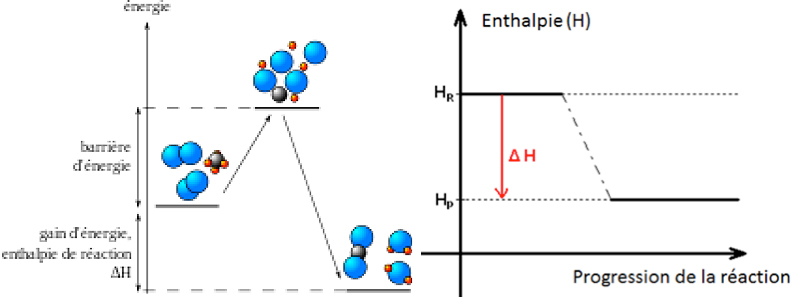
L’enthalpie est particulièrement importante lorsqu’il s’agit de décrire des transformations à pression constante. C’est notamment le cas de la plupart des réactions chimiques qui se déroulent à pression atmosphérique. La variation d’enthalpie est alors égale à la quantité de chaleur dégagée ou absorbée par le système, selon que la réaction est exothermique ou endothermique. Dès lors, une réaction exothermique se caractérise par le fait qu’elle produit de l’enthalpie et une réaction endothermique, par le fait qu’elle en consomme (Figure 11).
Cette représentation est caractéristique des moteurs thermiques qui exploitent largement le niveau d’enthalpie entre les gaz froids d’entrée d’admission (initiale) et la résultante lié à l’explosion des gaz de sortie (chauds). Le rendement thermodynamique des moteurs est étroitement lié à la relation volume / pression des gaz qui se traduit par un rapport volumétrique et un taux de compression des chambres de combustion.
3. Qu’est-ce qu’un combustible ?
Un combustible est un corps, une matière, un composé chimique qui a la propriété de brûler, en se combinant avec un comburant (comme le dioxygène O2) et une énergie thermique d’activation qui se consume dans une réaction chimique (oxydoréduction) en produisant de la chaleur par exothermie.
Les combustibles se présentent sous les trois états de la matière, à savoir : gazeux, liquide ou solide. Ils sont présents sur terre à l’état naturel ou transformés industriellement par l’homme. Leurs choix pour les différents usages sont liés aux domaines d’applications et aux pratiques culturelles et économiques locales qui sont multiples (Tableau 2).
Tableau 2 : Principaux combustibles
| Gazeux | Liquide | Solide |
| Méthane (CH4) gaz naturel | Pétrole brut | Tourbe |
| Acétylène (C2 H2) | Essence (produit de raffinage) | Lignite |
| Grisou (composé à plus 90% CH4) | Fuel lourd | Charbon maigre |
| Butane (C4 H10) | Fuel léger | Charbon gras |
| Propane (C3 H8) | Gas-oil | Anthracite |
| GPL (Gaz de Pétrole Liquéfié) | Kérosène | Bois (Brut) |
| Biogaz (issus des résidus agricoles) | Biocarburants (issus des végétaux) | Charbon de bois |
| Alcool | Végétal sec |
La combustion concerne donc les trois états de la matière et se traduit toujours par une mutation, liée à la réaction chimique d’oxydoréduction qui entraine une nouvelle construction moléculaire de la matière[1].
Les combustibles contiennent plus ou moins d’énergie et émettent plus ou moins de CO2, selon leur composition (Tableau 3).
Tableau 3 : Contenu énergétique des différents combustibles
| Combustible | Nombre de tep par tonne, m3, ou stère, selon le cas | MWh par tonne, m3, ou stère, selon le cas | |
| Essence (tonne) | 1, 048 | 12,2 | pour moteurs à essence |
| Gazole (tonne) | 1 | 11,6 | pour moteurs diesel |
| Fioul domestique (tonne) | 1 | 11,6 | pour chaudières |
| Ethanol (tonne) | 0,638 | 7,41 | alcool produit naturellement par fermentation |
| Agro diesel (tonne) | 0,876 | 10,2 | pour moteur Diesel |
| Gaz naturel (1000 m3) | 0,857 | 11,1 | la composition du gaz naturel est variable, % de méthane. |
| Charbon (tonne) | 0,619 | 7,20 | entre 6,2 et 7,6 selon la variété de charbon |
| GPL (tonne) | 1,095 | 12,73 | gaz de pétrole liquéfié, mélange de butane et propane |
| Butane (1000 m3) | 2,63 | 30,45 | 12,66 MWh par tonne |
| Propane (1000 m3) | 2,04 | 23,70 | 12,78 MWh par tonne |
| Bois (stère) | 0,147 | 1,71 | |
| Granulé de bois (tonne) | 0,39 | 4,5 | pour comparer le volume, par rapport au bois : 3,3 MWh/m3 |
| Hydrogène (tonne) | 2,86 | 33,25 | |
| Sources : Mémento du CEA, Comité National pour le Développement du Bois et Comité Français du Butane et du Propane. | |||
Une tonne d’essence contient 12,2 MWh. Avec une masse volumique de l’ordre de 750 kg/m3, un litre contient environ 750 g d’essence, soit 9,2 kWh ; un litre de fioul contient 10 kWh ; un litre de pétrole moyen aussi (Lire : Les unités d’énergie). En brûlant, tous les combustibles n’émettent pas des volumes identiques de CO2 (Tableau 4).
Tableau 4 : Emission de CO2 par les combustibles
| Combustible | kg de CO2 émis par kWh fourni |
| Essence | 0,264 |
| Gazole et Fioul domestique | 0,271 |
| Gaz naturel | 0,206 |
| Kérosène | 0,267 |
| Charbon | 0,343 |
| GPL | 0,231 |
| Déchets ménagers (fraction fossile) | 0,149 |
| Source : L’Agence de l’environnement et de la maîtrise de l’énergie (ADEME). | |
4. La combustion du bois énergie.
Le bois ne brûle pas spontanément, il doit passer par différentes phases avant d’entrer dans le processus de combustion (Lire : Biomasse et énergie). En prenant l’exemple de la combustion du bois buche utilisé pour le chauffage, une description complète de la combustion explicite les gradients de température dans les différentes phases qui conduisent à créer le processus de réaction chimique de combustion (Figure 12).
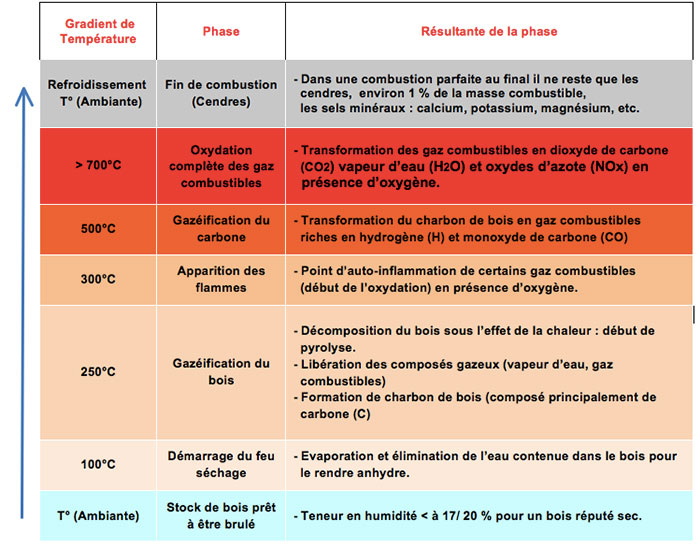
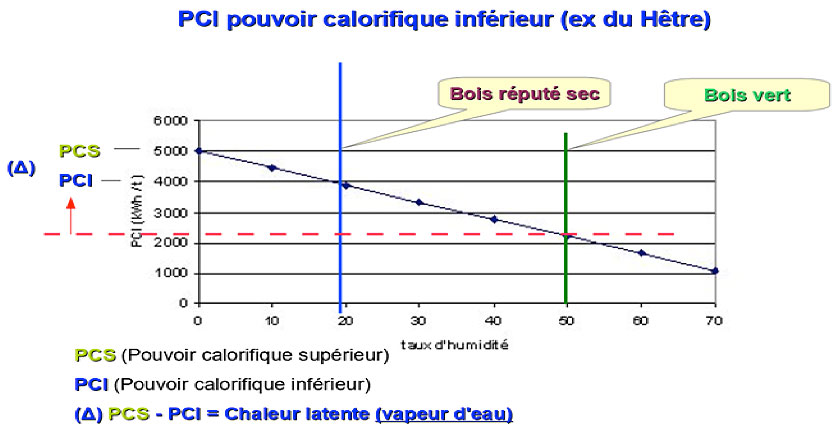
L’important est l’obtention d’une combustion complète du bois pour réduire les imbrulés et les rejets de fumées chargées de gaz polluants et de particules fines. Dans certaines régions, en fond de vallée, ces émissions sont à l’origine des pollutions d’hiver, lorsque la combustion est incomplète, en foyer ouvert ou mal adapté, non conforme aux règles de qualité du type label flamme verte, ou avec un taux d’humidité du bois trop élevé, lié à de mauvaises conditions de stockage, voire à du bois vert avec moins d’une année de séchage (Figure 13).
En théorie une combustion parfaite se traduit par très peu de cendres, environ 1% de la masse combustible, qui correspond à la matière incombustible, notamment les sels minéraux tels que calcium, potassium ou magnésium. Pour bruler du bois, il est donc impératif de respecter les règles fondamentales liées à la combustion et au prérequis concernant le stockage du combustible et la qualité du foyer utilisé.
Le bois énergie peut être une source d’énergie d’apport secondaire important, en combinant son usage avec celui d’autres sources d’énergie. En outre, il doit être mieux utilisé pour améliorer l’isolation des bâtiments, ce qui permet d’en réduire l’apport énergétique. Par définition, la combustion du bois par le feu pour produire des calories, plus exactement des thermies, n’est pas la solution d’avenir, mais plus on recule l’échéance d’améliorer l’efficience des bâtiments plus le coût augmente de même que les contraintes environnementale. De toute façon, mieux vaut utiliser du bois que des sources fossiles du type pétrole ou charbon.
Le bois présente en effet l’avantage d’être renouvelable et d’avoir un bilan carbone égal théoriquement à zéro puisque, lors de sa combustion, il restitue le carbone qu‘il a emmagasiné tout au long de sa vie, à condition de respecter l’espace temporel nécessaire à sa construction dans sa vie végétale.
De façon plus générale, l’usage du bois énergie doit s’intégrer dans la spécificité des exigences du moment, notamment des pays en voie de développement qui n’ont pas d’autre solution pour satisfaire leurs besoins énergétiques. C’est également vrai dans les pays industrialisés où des considérations économiques peuvent l’emporter sur le choix de l’efficience et des contraintes environnementales. La pédagogie, la communication vers le public utilisateur est importante. Ce qui est fondamental s’est d’être démonstratif car on imite plus facilement ceux qui proposent de bonnes solutions donnant de bons résultats que ceux qui sont liées à de mauvaises expériences !
5. Perspectives
Toutes les industries, les transports, le chauffage des bâtiments, l’agriculture, le confort des sociétés contemporaines, résultent de la combustion massive de sources d’énergie fossiles. Au 21ème siècle, la poursuite de la conversion par combustion de cette énergie chimique n’est plus viable au niveau planétaire, compte-tenu des dangers que constituent aussi bien les pollutions (SO2, NOx, particules fines) que les émissions de gaz à effet de serre (GES).
Dans la transition énergétique qui s’impose (Lire : La transition énergétique, un enjeu majeur pour la planète), les besoins des populations des pays en voie de développement notamment imposent de considérer avec la plus grande attention les usages du bois de chauffage et de ses dérivés. Utilisée à bon escient, la biomasse est en effet la source d’énergie la plus économique, la plus performante et la plus facile à mettre en œuvre dans bien des contrées du monde. Outre le bois de feu, le biogaz qui en est issu représente le combustible le moins polluant, tout en offrant de bons rendements énergétiques lors de sa conversion. Les bioéthanols peuvent aussi être des solutions transitoires pour une substitution aux produits fossiles tels que les dérivés pétroliers.
Dans ces domaines, comme dans bien d’autres, l’homme va devoir mettre toute son intelligence au service d’une volonté collective partagée pour faire avancer les changements indispensables à la sauvegarde d’une planète menacée. Nombre de défis sont à relever !
Notes et références
[1] Le terme combustible est aussi utilisé pour désigner la matière nucléaire fissile ou pouvant fusionner, mais les principes physico-chimiques de combustion sont bien différents des combustibles évoqués dans cet article. On peut aussi parler d’un autre combustible comme celui de l’hydrogène qui est utilisé dans les piles à combustibles, lequel repose aussi sur un autre principe physico-chimique
L’Encyclopédie de l’Énergie est publiée par l’Association des Encyclopédies de l’Environnement et de l’Énergie (www.a3e.fr), contractuellement liée à l’université Grenoble Alpes et à Grenoble INP, et parrainée par l’Académie des sciences.
Pour citer cet article, merci de mentionner le nom de l’auteur, le titre de l’article et son URL sur le site de l’Encyclopédie de l’Énergie.
Les articles de l’Encyclopédie de l’Énergie sont mis à disposition selon les termes de la licence Creative Commons Attribution – Pas d’Utilisation Commerciale – Pas de Modification 4.0 International.





