Dans la lente transition énergétique qu’entame le secteur du transport routier, l’hydrogène va probablement jouer un grand rôle. La technologie s’installe progressivement, mais, malgré une base technique solide, elle n’est pas encore compétitive à grande échelle et reste peu connue du grand public. Cet article présente la situation actuelle et les enjeux majeurs pour l’avenir.
Le transport routier a permis de repousser les limites de distance pour le développement économique et commercial des entreprises. Pour les citoyens, c’est un moyen de déplacement pratique, rapide et confortable qui permet en plus d’être indépendant. Les pays en développement, comme les pays industrialisés avant eux, ont bien compris ses atouts et son importance. Avec l’essor du pétrole au début du 20ème siècle, le moteur à explosion s’est imposé comme la solution la plus viable pour le développement industriel de l’automobile. Malheureusement quelques décennies plus tard, cette solution semble ne pas être aussi intéressante qu’à l’origine. En effet, ce type de moteur émet du dioxyde de carbone, l’un des principaux gaz à effet de serre (GES). Et pas dans une moindre mesure puisqu’en 2013, 27,6% des émissions de GES sont imputables au secteur des transports dont 92% pour le transport routier[1]. Et c’est bien sûr sans parler des particules fines qui sont un réel danger pour la santé.
Au vu de son rôle presque indispensable à la société et des investissements en infrastructures qui ont été réalisés, il est impossible de se passer du transport routier. Alors comment améliorer les véhicules pour continuer d’en profiter en réduisant drastiquement leur impact environnemental ? (Lire : Les sources d’énergie pour l’automobile du futur : les développements en cours et Les sources d’énergie pour l’automobile du futur : quelles options innovantes l’emporteront ?).
Les moteurs électriques sont une solution à ces problèmes. Néanmoins, ils soulèvent la question de la source d’énergie qui les alimentera, et des distances qu’ils permettront de parcourir. Si les batteries semblent être un moyen adapté, il n’est pas idéal sur plusieurs points comme l’autonomie, le prix, la masse à embarquer ou encore les matériaux utilisés. D’autres solutions sont donc envisagées dont l’une des plus prometteuse est celle qui fait appel au vecteur hydrogène[2] (Lire : L’hydrogène).
1. Qu’appelle-t-on un vecteur énergétique ?
C’est une forme d’énergie facilement transportable d’un point à un autre, utilisable ailleurs qu’en son lieu de production et qui peut éventuellement être stockée[3]. Ce n’est pas nécessairement une source d’énergie, même si ce peut-être le cas, comme le gaz transportable sous forme gazeuse dans des pipelines ou sous forme de gaz naturel liquéfié (GNL).
L’électricité est l’exemple le plus accompli de ce qu’est un vecteur énergétique. Les sources d’énergie nucléaires ou fossiles ne peuvent pas être déplacées facilement et/ou ne sont pas adaptées à l’utilisation finale souhaitée. De l’énergie est donc produite dans une centrale à l’aide de ces sources, que l’on transforme sous forme d’électricité via une génératrice. Cette électricité est facilement transportable par des lignes électriques jusqu’au consommateur final. Elle n’est pas utilisée en tant que telle mais transformée en lumière, en chaleur ou en énergie mécanique (Lire : L’électricité : éléments essentiels, génération et transport).
2. Le vecteur hydrogène pour faire tourner un moteur
Parmi les différents vecteurs énergétiques, l’hydrogène est l’un des plus intéressants.
2.1. Une alternative sérieuse aux carburants fossiles
Pour réussir la transition énergétique, il est nécessaire de trouver des formes d’énergie alternatives aux ressources fossiles (Lire : La transition énergétique : un concept à géométrie variable)
Fort d’un pouvoir calorifique élevé (environ 142 MJ/kg[4]), le dihydrogène a été initialement utilisé dans l’industrie spatiale comme combustible. À l’instar d’autres technologies utilisées dans des domaines de pointe, les études et les progrès techniques sur le transport, le stockage et plus généralement l’utilisation de l’hydrogène ont permis de découvrir son potentiel de vecteur énergétique. C’est aujourd’hui le domaine des transports routiers qui, pour en terminer avec l’usage de carburants issus du pétrole et du gaz, commence à utiliser l’hydrogène pour la motorisation. On recense deux technologies principales[5], la première étant l’utilisation de l’hydrogène comme combustible dans un moteur à explosion, la seconde étant la pile à combustible (Lire : Les piles à combustible).
2.2. Utiliser l’hydrogène comme carburant dans un moteur thermique
Cette solution est assez intuitive puisqu’elle consiste simplement à utiliser l’hydrogène comme carburant dans un moteur thermique, à l’instar du gazole ou de l’essence aujourd’hui. Si l’on peut utiliser l’hydrogène seul, l’intérêt principal de cette technologie réside dans le fait qu’elle permettrait de créer des véhicules hybrides hydrogène/essence ou hydrogène/gazole. Même si ce n’est pas une solution désirable à long terme, son utilisation pour aider la transition énergétique dans le domaine des transports, pourrait être envisageable.
Quelques véhicules ont été fabriqués avec cette technologie, comme la BMW Hydrogen 7, abandonnée par la marque allemande. L’explication est en partie technique ; l’hydrogène possède une faible énergie d’inflammation ce qui signifie que lorsqu’il est soumis aux températures et pressions élevées dans un cylindre du moteur, il peut s’auto-enflammer. Ainsi, un phénomène de cliquetis[6] peut apparaître et détériorer les composants du moteur. De plus, l’acier ne résistant pas aux températures atteintes, une culasse en céramique aurait été nécessaire. Cette option étant trop coûteuse, le choix a été fait de faire fonctionner le moteur à plus basse température en diminuant le rendement de Carnot et donc le rendement maximal atteignable. Enfin, une rentabilité incertaine et des stations de recharge encore trop rares ont joué en défaveur de cette technologie.
Les perspectives pour l’avenir semblent donc se trouver dans la pile à combustible.
2.3. Produire de l’électricité à partir de l’hydrogène: la pile à combustible (PAC)
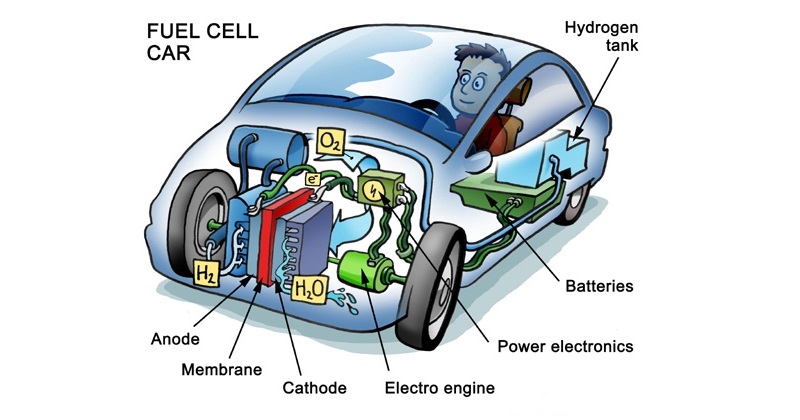
Les progrès sur ce type de technologie permettent d’utiliser aujourd’hui l’hydrogène pour des véhicules : en faisant réagir du dihydrogène et du dioxygène de l’air, la pile à combustible permet de faire circuler un courant électrique dans les électrodes d’une PAC. Ce courant servira ensuite à alimenter un moteur électrique.
Entre les divers types de piles à combustibles, qui toutes n’utilisent pas forcément l’hydrogène, les PAC à hydrogène ont l’avantage de ne produire que de l’eau et de la chaleur. Elles sont en outre techniquement les plus simples à mettre en œuvre.
La seule famille aujourd’hui commercialement mature et utilisée dans les véhicules est la PEMFC (Proton Exchange Membrane Fuel Cell – PAC à membrane échangeuse de protons). Les autres technologies font face à des verrous techniques encore non résolus ou à des problèmes de coûts et de disponibilité de la ressource liés à la présence du platine (Pt) dans les électrodes. Ce dernier est néanmoins présent dans les PEMFC, mais dans une proportion suffisamment faible pour autoriser des coûts acceptables et être utilisable à grande échelle (Figure 1).
À l’anode a lieu une réduction :
O2(g) + 4H+(aq) + 4e– → 2H2O(l) (1)
À la cathode, c’est une oxydation du dihydrogène :
H2(g) → 2H+(aq) + 2e– (2)
L’équation bilan est donc :
H2(g) + ½ O2(g) → H2O(l) (3)
Pour dimensionner une pile à combustible et connaître la quantité d’hydrogène nécessaire pour une autonomie donnée, il faut d’abord déterminer le courant nominal du moteur. Ensuite, la loi de Faraday donne le flux molaire d’hydrogène nécessaire et ainsi la quantité totale à embarquer.
FH2=I/nF (4)
La donnée n correspond au nombre d’électrons échangés en consommant une mole d’H2 lors de la réaction. Comme exposé dans l’équation (2), on a n = 2.
En général, la consommation de carburant dans des conditions de circulation fluide en ville ou en campagne est de l’ordre de 0,8kg/100km en prenant en compte un rendement de la pile à combustible compris entre 40 et 60% et un taux d’utilisation autour de 90%[7].
Au vu des nombreuses recherches conduites sur les PAC, on peut s’attendre à l’amélioration de leurs performances et notamment à l’arrivée sur le marché d’autres types de piles à combustible aujourd’hui en développement. Parmi elles, les SOFC (Solid-Oxyde Fuel Cell) qui sont des PAC à oxyde solide présentant de nombreux atouts par rapport aux PEMFC. Elles ont la particularité de fonctionner à des températures de l’ordre de 500 à 1000°C ce qui leur donne l’avantage de ne pas nécessiter de catalyseur précieux comme le platine ou d’avoir une taille réduite de l’échangeur thermique nécessaire à l’évacuation de la chaleur libérée par la PAC. Par ailleurs les SOFC peuvent être alimentées avec une multitude de combustibles ce qui leur donnerait une flexibilité intéressante dans des véhicules.
3. Méthodes de production de l’hydrogène pour un véhicule respectueux de l’environnement
L’hydrogène est un élément présent en abondance sur terre, mais il n’existe à l’état naturel qu’en petite proportion souvent non récupérable[8]. À l’instar de la molécule d’eau H2O, un atome d’oxygène et deux d’hydrogène, ce dernier est présent sous forme combinée avec d’autres éléments. Il doit donc être produit à partir de ces molécules ce que permettent de nombreux procédés. Tous ne sont cependant pas respectueux de l’environnement, tels ceux utilisés dans l’industrie qui le produit à plus de 90% du temps par des procédés à base d’hydrocarbures, donc polluants et inadaptés aux véhicules du futur.
Des méthodes de production d’hydrogène propre existent mais elles-mêmes doivent respecter certaines conditions. Tout d’abord, l’utilisation de biométhane ou de biomasse solide peut être une solution faiblement émettrice de CO2. Il existe également plusieurs procédés dits verts car ils n’émettent pas de polluants mais un seul est aujourd’hui au stade de commercialisation: l’électrolyse[9] (Lire : La production d’hydrogène « vert »).
3.1. Vaporeformage du biométhane
Le vaporeformage du gaz naturel (eq.5) est aujourd’hui à l’origine de la plus grande partie de l’hydrogène utilisé pour l’industrie chimique (production d’ammoniac) ou le raffinage du pétrole. Il fait réagir du méthane et de la vapeur d’eau à haute température (>800°C) et sous une pression de 10 à 40 bars[10].
CH4(g) + H2O(g) → CO(g) + 3H2(g) (5)
L’usage d’un catalyseur judicieusement choisi permet d’améliorer la cinétique de la réaction de reformage et d’en diminuer la température, ce qui améliore le rendement de la réaction.
Une part plus grande d’hydrogène peut être collectée à l’aide d’une seconde réaction à partir du monoxyde de carbone produit par le reformage. Cette « réaction du gaz à l’eau » (Water-Gas-Shift , eq.6) se produit à une température plus faible que précédemment (ordre de grandeur 200-400ºC) et produit du dioxyde de carbone gazeux dont il faudra se débarrasser.
CO(g) + H2O(g) → CO2(g) + H2(g) (6)
Utiliser du gaz naturel présent dans le sol provoque des émissions de gaz à effet de serre.
La méthanisation de déchets organiques produit du biogaz, composé de méthane à hauteur de 60% environ. Ce biogaz est épuré afin de supprimer une partie des autres gaz présents et obtenir un biométhane aux propriétés semblables au gaz naturel. L’intérêt de la méthanisation est de valoriser les déchets liés à nos activités et produire un méthane au bilan carbone a priori neutre. Par ailleurs, une réaction de reformage à sec du méthane (eq.7) existe aujourd’hui, en le faisant réagir avec du CO2.
CH4(g) + CO2(g) → 2CO(g) + 2H2(g) (7)
Cette réaction a un double intérêt par rapport au vaporeformage, puisqu’elle peut utiliser directement le CO2 contenu dans le biogaz, et qu’en plus de ne pas produire ce gaz à effet de serre, elle le consomme. Cette solution est actuellement testée en laboratoire.
3.2. Gazéification du charbon de bois
Le charbon de bois est obtenu en faisant subir des transformations à la biomasse. Premièrement la biomasse est séchée afin d’évacuer l’humidité qu’elle contient par évaporation. Ensuite, la biomasse sèche subit une opération de pyrolyse qui consiste à la chauffer à une température généralement comprise entre 300°C et 700°C afin d’extraire les matières les plus volatiles et obtenir un composé très carboné et poreux : le char. Ce dernier subit à son tour des transformations supplémentaires pour être gazéifié. Les matières volatiles subissent une combustion qui va permettre d’atteindre une température élevée dans le réacteur et de produire de la vapeur d’eau et du CO2. Ce sont ces deux derniers qui vont réagir à haute température (~1000°C) avec le carbone du charbon de bois pour produire du syngaz composé d’hydrogène et de monoxyde de carbone[11]. Les équations de la gazéification de la biomasse sont les suivantes :
Gazéification à la vapeur d’eau :
C(s) + H2O(g) → CO(g) + H2(g) (8)
Gazéification au dioxyde de carbone :
C(s) + CO2(g) → 2CO(g) (9)
La cinétique de cette dernière réaction étant deux à cinq fois plus lente que la première, la gazéification à la vapeur d’eau est prépondérante.
La biomasse inclut le bois mais aussi différents types de déchets agricoles, animaux ou industriels, valorisables sous forme d’énergie. Les résidus végétaux absorbent a priori la même quantité de carbone que celle qu’ils relâchent, et la valorisation des déchets reste une solution très intéressante pour limiter le gaspillage et la pollution. Néanmoins, la déforestation étant déjà en cours à l’échelle mondiale, l’utilisation du bois pour la production d’hydrogène peut être contestée, sauf si la reforestation, l’utilisation raisonnée du bois et l’amélioration des rendements autorisent à classer ce type de biomasse comme une source d’énergie renouvelable.
3.3. L’électrolyse
Plusieurs technologies existent, avec différents éléments comme l’électrolyse chlore-soude dont l’hydrogène est un produit fatal[12], mais la plus propre et la plus adaptée au cas étudié est l’électrolyse de l’eau. Le principe de celle-ci est de fournir de l’énergie électrique à l’eau pour produire de l’hydrogène et de l’oxygène. (Figure 2).
À l’anode a lieu une oxydation des ions hydroxyde (HO–) :
2H2O(l) → O2(g) + 4H+(aq) + 4e– (10)
À la cathode, c’est une réduction du dihydrogène :
2H+(aq) + 2e– → H2(g) (12)
L’équation bilan est donc :
H2O(l) → H2(g) + ½ O2(g) (11)
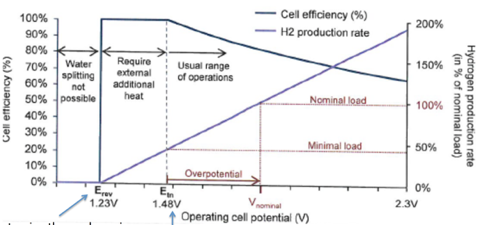
La figure ci-jointe donne quelques caractéristiques théoriques du fonctionnement de l’électrolyse dans les CNTP (cf. note bas de page 2). Plusieurs points importants sont à souligner.
Premièrement, la réaction ne peut pas se produire si la tension de cellule est inférieure à 1,23Vdc. Cette valeur appelée tension thermodynamique correspond à la variation d’enthalpie libre ΔGd, soit la quantité minimale d’énergie électrique à fournir. Elle est calculée avec la formule suivante :
E=ΔGd/nF
avec n le nombre de moles d’électrons échangés pour une mole d’hydrogène produite (2 pour l’électrolyse de l’eau) et F le nombre de Faraday.
Cette réaction comporte cependant des irréversibilités nécessitant un apport supplémentaire de chaleur. La variation d’entropie ΔS est strictement positive. Or, l’enthalpie de réaction ΔHd = ΔGd + TΔS. Ceci se traduit par une augmentation de la tension nécessaire. On introduit alors la tension thermo-neutre V= ΔHd/nF soit 1,48Vdc.
Dans ces conditions l’efficacité de la cellule, définie comme le rapport de l’énergie utile à la réaction sur l’énergie fournie est théoriquement de 100% à courant nul. Néanmoins le taux de production d’hydrogène est assez faible dans ces conditions. Dans le milieu industriel, la tendance est d’imposer la tension des cellules entre 1,7Vdc et 2,1Vdc[13] afin d’obtenir un meilleur compromis entre efficacité et production. Une partie de l’énergie électrique fournie ne sera pas utile à la réaction mais va apporter de la chaleur qu’il faudra évacuer afin de maintenir le réacteur à une température acceptable (Figure 3).
Si l’objectif est bien de produire de l’hydrogène avec des méthodes respectueuses de l’environnement, les moyens de production de l’électricité nécessaire à l’électrolyse doivent donc être déterminés dans une optique renouvelable. Aujourd’hui, les centrales à combustible fossile restent majoritaires pour cette application en raison des hautes puissances demandées en continu par l’électrolyse et des quantités nécessaires. Joue aussi l’héritage historique des industries, chimique et pétrochimique, qui restent encore les principaux consommateurs d’hydrogène. Néanmoins la volonté est là et des projets de fermes éoliennes et/ou solaire couplées aux électrolyseurs sont déjà réalisés, à l’instar du projet Myrte en Corse[14] faisant intervenir l’université de Corse, une filiale d’Areva et le Commissariat à l’énergie atomique (CEA). Dans le cadre de ce projet, des panneaux photovoltaïques ont été couplés à un électrolyseur pour stocker de l’énergie sous forme d’hydrogène et la restituer à l’aide d’une pile à combustible.
3.4. D’autres procédés verts pour l’avenir
Produire de l’hydrogène vert en grandes quantités est désormais un enjeu suffisamment important pour que plusieurs procédés fassent l’objet de recherche dans l’espoir d’être industriellement réalisables à grande échelle. Parmi eux[15] :
- la photo-électrolyse de l’eau qui consiste à fournir de l’énergie aux électrons d’un matériau semi-conducteurs grâce à des photons et à déclencher une réaction d’électrolyse comme vu précédemment ;
- la dissociation thermo-chimique de l’eau : à l’aide d’une centrale solaire thermodynamique à concentration ou d’un réacteur nucléaire pouvant élever fortement la température de l’eau et en ajoutant des substances chimiques pour faciliter la réaction, il est possible de séparer la molécule d’eau en un atome d’hydrogène et un atome de dioxygène.
- à partir de la photosynthèse de certaines algues vertes et cyanobactéries qui permet de produire de l’hydrogène par une suite de procédés biologiques.
4. Stocker de l’hydrogène à bord d’un véhicule
Le stockage de l’hydrogène embarqué est l’une des difficultés principales puisqu’il est soumis à plusieurs conditions contraignantes : pouvoir le stocker en quantité suffisante pour obtenir une autonomie raisonnable ; le faire dans un réservoir le plus petit possible et facilement installable dans le véhicule ; le tout en assurant la sécurité des personnes et du matériel. Pour ce faire, les technologies envisagées sont le stockage sous forme gazeuse, liquide ou solide.
4.1. La solution actuelle : le stockage sous forme gazeuse
Les véhicules fonctionnant à l’hydrogène en 2017 sont tous dotés d’un réservoir d’hydrogène gazeux. Le problème que soulève cette solution est sa faible masse volumique. Pour embarquer une quantité suffisante de carburant, soit généralement entre 2 et 5 kg, il est alors nécessaire de comprimer l’hydrogène à une pression comprise entre 350 et 700 bars pour limiter le volume occupé par le réservoir. Par ailleurs, l’atome d’hydrogène étant très petit, son noyau n’étant constitué que d’un seul proton, le risque de fuite est élevé. Or, l’hydrogène peut s’enflammer facilement et parfois provoquer une explosion au contact du dioxygène si sa proportion est comprise entre 4 et 75% dans un mélange avec de l’air[16]. Les réservoirs n’étant pas conservés dans l’habitacle mais à l’extérieur sous le véhicule, le risque provient surtout d’une rupture brutale de l’enceinte.
Il est donc nécessaire d’utiliser des matériaux pouvant soutenir les hautes pressions et suffisamment solides pour résister à des impacts. En cas d’incendie, une soupape de sécurité permet de limiter l’augmentation de pression liée à l’échauffement du gaz et donc d’éviter l’explosion du réservoir. De plus, des capteurs permettent de vérifier l’absence de fuite de carburant qui pourrait toujours provoquer une perte d’autonomie.
4.2. Le stockage d’hydrogène liquide
En le refroidissant à très basse température, environ -250ºC[17], l’hydrogène passe à l’état liquide. Cette propriété permet de stocker l’hydrogène avec une bonne densité volumique, meilleure que celle de l’état gazeux. Néanmoins, la mise en place de cette solution est complexe ; elle demande de grandes quantités d’énergie pour refroidir le gaz et une excellente isolation du réservoir. Sa faisabilité est prouvée puisque cette technologie est utilisée dans l’industrie spatiale mais l’évaporation de l’hydrogène est inévitable, un calorifugeage parfait étant impossible, et reste le problème majeur de cette technologie. Enfin, aux coûts trop élevés pour une application automobile, s’ajoutent les risques liés, entre autres, à la pression de plusieurs dizaines de bars dans le réservoir.
4.3. Le stockage sous forme solide
L’idée est de stocker l’hydrogène sous forme d’hydrures métalliques (de l’ion hydrure H–) en le faisant absorber par un composé métallique. Cette solution est plus sécurisée que les deux précédentes en limitant la pression et en évitant la cryogénie. Elle présente une bien meilleure densité volumique que la solution gazeuse notamment.
Une PME française, McPhy Energy, en partenariat avec le CNRS et le CEA a réussi à déposer un brevet pour une solution utilisant le magnésium en vue de fixer l’hydrogène. La récupération de ce dernier s’effectue en chauffant le composé, pour un rendement global de 90%. Cette entreprise a déjà un démonstrateur en fonctionnement pouvant stocker jusqu’à 3,3 MWh[18]. Pour lever des fonds supplémentaires et accélérer le développement de cette solution qui semble prometteuse, l’entreprise McPhy Energy a été introduite en bourse. Enfin, cette solution s’annonce également viable d’un point de vue économique avec un prix de production estimé à cinq euros par kilogramme d’hydrogène[19].
Cette méthode de stockage possède cependant un fort inconvénient, qui est son rendement massique de 5 à 6% ce qui se traduit par une masse de matériau absorbant vingt fois supérieure à la masse d’hydrogène stockée et donc à un véhicule significativement plus lourd.
En résumé, les différents niveaux de la masse volumique de l’hydrogène pour chaque technologie de stockage prouvent l’intérêt de poursuivre les recherches pour le stockage liquide ou solide :
– stockage d’hydrogène sous forme de gaz (700 bars) : 42kg / m3
– stockage d’hydrogène sous forme liquide : 70kg / m3
– stockage d’hydrogène sous forme solide MgH2 : 106kg / m3.
5. Recharger un véhicule à hydrogène
Les difficultés techniques, passées en revue, rendent difficiles l’intégration à bord d’un véhicule de l’un des procédés pour produire de l’hydrogène en respectant l’environnement. Un temps considérée, l’électrolyse a été rapidement abandonnée puisqu’il n’y aurait pas intérêt à utiliser une batterie pour la faire fonctionner. Il est donc nécessaire de recharger les véhicules dans des stations comme c’est le cas aujourd’hui pour le gazole et l’essence. La solution envisagée est de conserver l’hydrogène dans de grands réservoirs à haute pression, généralement une centaine de bars au dessus de la pression à délivrer (350 ou 700 bars) comme évoqué précédemment, pour ensuite leur connecter les véhicules qui se rechargeront.
Lors d’une recharge, la pression du réservoir amont diminue. Or, si la cadence de véhicules est supérieure à la vitesse de remplissage du réservoir amont, la pression dans celui-ci va diminuer constamment et la recharge du véhicule s’arrêtera quand les pressions du réservoir de la station et de celui du véhicule seront égales, sans recharger le véhicule complètement. Par ailleurs, compresser de grands volumes de gaz exige une quantité d’énergie non négligeable qui augmente avec la pression. Pour compresser de l’hydrogène à 700 bars, environ 30% de l’énergie consommée sont des pertes. Ce qui reste inférieur aux 50% de pertes lors de la liquéfaction de l’hydrogène. Certains électrolyseurs fonctionnent cependant à haute pression (jusqu’à 35 bars) ce qui permet de diminuer la surpression à fournir au gaz. Des améliorations sont donc également nécessaires pour optimiser la phase de recharge.
6. Un exemple concret : Symbio
Pionnière et bien installée sur le marché des véhicules à hydrogène, Symbio est souvent citée en exemple. Ses activités principales sont la conception et la fabrication de véhicules dotés de piles à combustibles, ou bien de kits de piles à combustibles, alimentés par de l’hydrogène et pouvant être intégrés dans des véhicules tels qu’utilitaires, bus, poids lourds ou encore bateaux.
6.1. Les réalisations de l’entreprise
Elles appartiennent à deux familles.
- Les prolongateurs d’autonomie
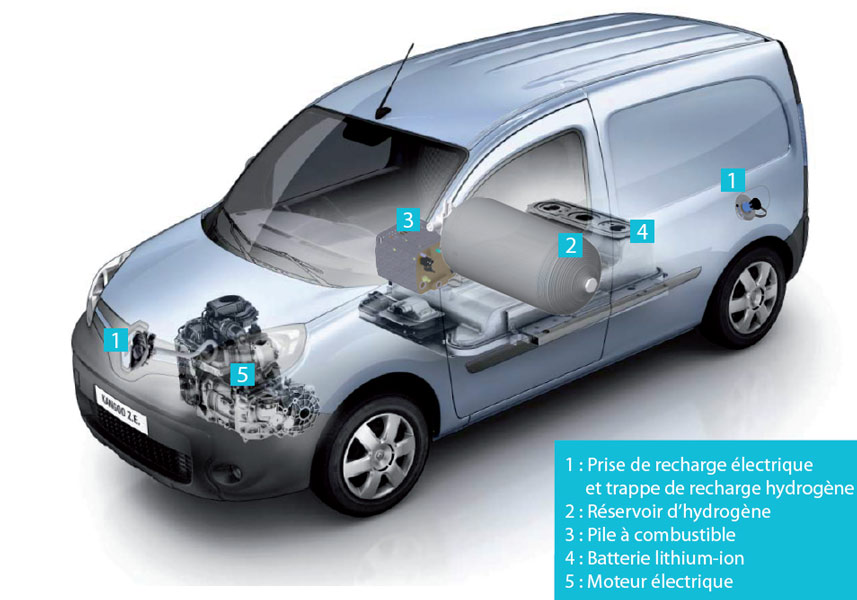
Solution phare de l’entreprise, elle consiste à prolonger l’autonomie d’un véhicule électrique en combinant l’usage de l’hydrogène et de batteries. Deux types de montages existent: un montage série dans lequel l’hydrogène recharge la batterie (Figure 4) qui est la source principale ou bien un montage parallèle utilisant l’hydrogène comme source principale.
- Les véhicules à hydrogène seul
Ce type de véhicule fonctionne uniquement grâce à une pile à combustible et à un stockage d’hydrogène gazeux pour alimenter un moteur électrique. Cette solution a été appliquée à la Green GT-H2, prototype de compétition de la société Green GT, qui est l’un des premiers véhicules sur lequel Symbio a travaillé. Ce prototype reste une exception. Tous les véhicules mis sur le marché sont équipés de batteries, l’hydrogène étant utilisé comme prolongateur d’autonomie.
La première solution semble être la plus intéressante pour proposer des véhicules disposant d’une plus grande autonomie et d’une plus large polyvalence d’utilisation. Puisqu’il est peu intéressant d’avoir un système d’électrolyse à bord du véhicule, il est impossible de récupérer l’énergie du freinage dans un véhicule fonctionnant sans batterie. À l’inverse, la batterie est plus adaptée pour un usage citadin que pour des longs trajets à vitesse élevée. L’usage de l’hydrogène permet de faciliter cette utilisation du point de vue technique mais l’intérêt économique est encore à prouver[20]. Un autre avantage de l’hydrogène est le temps de recharge ; quelques minutes, comme pour les moteurs thermiques, contre plusieurs heures pour une batterie.
L’usage de deux sources d’énergie augmente donc la fiabilité du système, mais la disponibilité des stations doit tout de même être suffisante pour obtenir la confiance des utilisateurs en vue d’un développement à grande échelle.
En 2017, le véhicule phare de Symbio est la Kangoo ZE-H2, version améliorée de la Kangoo électrique de Renault, déjà en service en France et utilisée notamment par La Poste (Figure 4). Les projets pour les années à venir sont des prolongateurs d’autonomie pour des véhicules plus lourds : des utilitaires électriques d’une masse de 3,5 tonnes maximum contre 2,2 pour la Renault ZE, des bus et même des camions-bennes. Par ailleurs Symbio utilise aujourd’hui des réservoirs d’hydrogène pressurisé à 350 bars mais des modèles à 700 bars sont prévus pour bientôt.
6.2. Organisation et gestion de l’innovation
Symbio est une start-up Grenobloise fondée en 2010. Elle s’est construite sur les recherches du CEA en matière de pile à combustible pour l’automobile. La branche investissement du CEA fut par ailleurs le premier actionnaire de Symbio. Si l’entreprise possède son propre bureau d’études, le CEA continue d’apporter son aide sur certaines missions de recherche et développement. Par la suite, l’entreprise a conclu un partenariat avec Renault, lançant l’activité pour les véhicules utilitaires Kangoo ZE-H2. Michelin et plus récemment (2016) Engie sont devenus également actionnaires. Les financements de Symbio sont donc principalement d’origine privée.
L’entreprise a déjà délivré plus de cent exemplaires de sa Renault ZE-H2, à des entreprises comme La Poste mais aussi à des acteurs publics à l’instar de l’Élysée et de la Métropole de Grenoble dans le cadre du projet H2mobility[21]. Elle exploite également une station de recharge à Grenoble. Le prix de l’hydrogène dans la plupart des stations existantes aujourd’hui est compris entre huit et dix euros par kilogramme. Ceci représente moins de 20 euros pour un plein assurant un peu moins de 200km d’autonomie, ce qui ajouté à celle de la batterie, donne un total d’environ 300km d’autonomie.
Si ces véhicules restent trop onéreux pour un particulier, car fabriqués en petites séries, ils présentent un intérêt grandissant pour une flotte de véhicules professionnels, avec un coût global d’utilisation se rapprochant de celui d’une flotte diesel.
Pour que cette solution de transport se diffuse, l’implantation de stations de recharge sur tout le territoire s’impose, ce qui représente de lourds investissements estimés à des montants compris entre 200 000 et 1 million d’euros. La confiance dans le futur de cette technologie permet cependant que subventions soient débloquées par les acteurs publics, comme la Commission Européenne pour le projet EAsHyMob[22].
Preuve de sa réussite et de sa reconnaissance internationale, Symbio est citée dans de nombreux articles sur le sujet et était présente au Consumer Electronics Show (CES) de Las Vegas, début janvier 2017.
7. Conclusion générale
Les véhicules à hydrogène n’ont pas encore atteint la maturité économique et sociale leur permettant d’être développés à grande échelle. Les industriels et les laboratoires de recherche continuent de développer cette technologie pour améliorer ses performances et diminuer ses coûts, tandis que plusieurs start-ups s’appuient avec succès sur eux pour lancer ce qui deviendra peut-être le futur de nos transports routiers. Ces derniers devront être véritablement respectueux de l’environnement, notamment sous la forme d’un hydrogène issu de filières décarbonées et durables.
Une large marge de progression existe pour rendre cette technologie plus facile à implanter dans les véhicules et surtout pour réduire leurs coûts et permettre leur démocratisation.
Aux côtés des véhicules individuels, des transports en commun intelligents fonctionnant à l’hydrogène apparaissent comme une piste sérieuse pour transformer les moyens de déplacement dans le sens de la transition énergétique.
Notes et références
[1] Données du ministère des transports. http://www.developpement-durable.gouv.fr/Transports,34304.html [consulté le 23/12/2016]
[2] Notons que l’entité véritablement utilisée dans les applications est le dihydrogène (H2), forme moléculaire stable de l’élément hydrogène (H) dans les conditions normales de température et de pression, en abrégé, CNTP soit une pression de 1 bar et une température de 20°C. Par commodité, le terme hydrogène sera employé par la suite.
[3] Cf. « les vecteurs d’énergie ». http://web.archive.org/web/20071130125033/www.academie-technologies.fr/publication/rapports/energieEnvironnement/syntheseEE2004/ann9.pdf [consulté le 23/12/2016]
[4] La comparaison avec le méthane montre la densité énergétique massique importante pour l’hydrogène.
http://eduscol.education.fr/orbito/pedago/pileh2/pile31.htm [consulté le 26/12/2016]
[5] Cf. « technologies existantes ».
http://www.connaissancedesenergies.org/fiche-pedagogique/hydrogene-dans-les-transports [consulté le 26/12/2016]
[6] Quelques éléments d’explication sur le cliquetis dans les moteurs à hydrogène dans la partie I:
http://www.cder.dz/vlib/bulletin/pdf/bulletin_019_08.pdf [consulté le 23/03/2017]
[7] Une partie de l’hydrogène n’est pas utilisée pour la réaction mais pour évacuer l’eau produite à l’anode. On introduit donc plus d’hydrogène que la quantité nécessaire, le taux d’utilisation étant le taux d’hydrogène utile à la réaction chimique.
[8] Si l’on ne considérait auparavant que sa présence infime dans l’atmosphère, de nouvelles sources naturelles d’hydrogène ont été découvertes. Dans les années 1970, des preuves d’émanation d’hydrogène dans les océans ont été apportées. Cependant, ces dernières étaient d’une ampleur modérée et surtout en profondeur donc difficilement récupérables. Plus récemment, l’existence de gisements d’hydrogène dans le sol terrestre a été démontrée et les industriels, bien que prudents, s’y intéressent.
https://www.industrie-techno.com/l-hydrogene-naturel-future-source-d-energie.42054 [consulté le 28/12/2016]
[9] Les procédés de production d’hydrogène peuvent être rendus plus propres en utilisant des réactifs non fossiles. D’autres procédés n’utilisant pas de composés carbonés sont également à l’étude. Un état des lieux succinct mais précis de la situation aujourd’hui: http://www.planete-energies.com/fr/medias/decryptages/comment-fabriquer-l-hydrogene [consulté le 29/12/2016]
[10] Thése sur la production d’hydrogène par vaporeformage du methane. https://tel.archives-ouvertes.fr/tel-00828240/document [consultée le 29/12/2016]
[11] http://www.gazeification.info [consulté le 29/12/2016]
[12] Un produit est dit fatal s’il n’est pas utile pour l’application désirée mais est obtenu nécessairement lors de la réaction.
[13] Ces valeurs de tension ainsi que les données sur les potentiels thermodynamiques et thermoneutres dans les CNTP obtenues sur http://mon.univ-montp2.fr/claroline/backends/download.php?url=L0VsZWN0cm9seXNlLnBkZg%3D%3D&cidReset=true&cidReq=GMCH213_002 [consulté le 29/12/2016]
[14] http://www.20minutes.fr/planete/855688-20120109-projet-myrte-va-eclairer-corse, [consulté le 09/02/2017]
[15] Plus d’informations disponibles sur https://www.encyclopedie-energie.org/la-production-d’hydrogène-«-vert-», [consulté le 27/12/2016] et sur les fiches de l’AFHyPAC, onglet « production d’hydrogène » : http://www.afhypac.org/documentation/tout-savoir/ [consulté le 27/03/2017]
[16] http://www.afhypac.org/documents/tout-savoir/fiche_7.1_inflammabilite_explosivite_rev._fev_2015_ineris_bwe_pm.pdf , [consulté le 9/02/2017]
[17] Pour rappel, le “zéro absolu”, ou la température la plus basse qu’un système physique puisse atteindre est environ de -273,15ºC.
[18] https://www.lenergieenquestions.fr/utiliser-lhydrogene-pour-stocker-lenergie-la-solution-de-mcphy-energy/, [consulté le 10/02/2017]
[19] https://www.contrepoints.org/2014/03/10/159061-stocker-les-energies-renouvelables-grace-a-lhydrogene-solide, [consulté le 11/02/2017]
[20] http://www.usinenouvelle.com/article/le-vehicule-electrique-a-hydrogene-pour-les-nuls.N294150, [consulté le 11/02/2017]
[21] Informations sur le contenu et les acteurs du programme « Mobilité Hydrogène France » http://www.plateformesolutionsclimat.org/wp-content/uploads/2015/04/H2-Mobilit—France-FR-v19.pdf [consulté le 02/04/2017]
[22] http://pole-moveo.org/actualites/1ere-mondiale-un-reseau-de-stations-de-recharge-hydrogene-en-basse-normandie/ [consulté le 12/02/2017]
L’Encyclopédie de l’Énergie est publiée par l’Association des Encyclopédies de l’Environnement et de l’Énergie (www.a3e.fr), contractuellement liée à l’université Grenoble Alpes et à Grenoble INP, et parrainée par l’Académie des sciences.
Pour citer cet article, merci de mentionner le nom de l’auteur, le titre de l’article et son URL sur le site de l’Encyclopédie de l’Énergie.
Les articles de l’Encyclopédie de l’Énergie sont mis à disposition selon les termes de la licence Creative Commons Attribution – Pas d’Utilisation Commerciale – Pas de Modification 4.0 International.


![Fig. 1 : Schéma de principe d’une PEMFC. - Source : By Nécropotame [FAL], from Wikimedia Commons](https://www.encyclopedie-energie.org/wp-content/uploads/2017/04/art133_figure1_principe-pemfc.jpg)
![Fig. 2 : Schéma de principe d’une électrolyse. L'eau n’étant pas conductrice par nature, elle doit être dopée avec des conducteurs ioniques pour que l’électrolyse fonctionne - Source : By Jn gautier (Own work) [CC BY-SA 3.0 (http://creativecommons.org/licenses/by-sa/3.0)], via Wikimedia Commons](https://www.encyclopedie-energie.org/wp-content/uploads/2017/04/art133_figure2_principe-electrolyse.jpg)