Pour occuper la place qui lui est promise dans la transition énergétique, la ressource biomasse devra être en grande partie traitée pour améliorer son contenu énergétique, notamment via la gazéification. Mais qu’est-ce que la gazéification ? Quelles réactions chimiques implique-telle ? Qu’attendre des divers types de dispositifs (lits fixes, lits fluidisés, réacteur à flux entraînés) ? Quelles sont les principales réalisations en cours ?
La forme solide sous laquelle se présentent certaines ressources énergétiques relativement abondantes, telles que la biomasse ou le charbon minéral, ne se prête pas à une utilisation aisée car leur transport, leur stockage et, surtout, l’alimentation des différentes machines énergétiques (moteurs, fours ou chaudières) soulèvent de nombreuses difficultés. Il est donc tentant d’essayer de transformer ces ressources en une forme plus facilement utilisable comme un gaz ou un liquide. Tel est l’objectif de la gazéification.
1. Qu’est-ce que la gazéification ?
La gazéification est la transformation thermique et chimique d’un matériau solide tel que le charbon ou la biomasse essentiellement formés de carbone (C), d’hydrogène (H) et d’oxygène (O)) en présence d’un réactif gazeux (oxygène, vapeur d’eau, hydrogène, entre autres). Elle est donc différente de la pyrolyse (ou thermolyse) qui est un processus thermique réalisé en l’absence de gaz de réaction. La gazéification consiste donc à convertir du solide en un mélange gazeux, appelé gaz de synthèse (syngas), contenant principalement les espèces hydrogène (H2), méthane (CH4), monoxyde de carbone (CO), dioxyde de carbone (CO2) et vapeur d’eau (H2O) dans des proportions dépendant du procédé, dont les performances sont fonction à la fois des caractéristiques du solide à transformer et de l’utilisation finale du gaz de synthèse.
Le mélange gazeux obtenu peut en effet être utilisé pour différentes applications que sont notamment la production de gaz combustible et la synthèse de biocarburants.
Le gaz combustible a été utilisé dans un moteur pour la traction automobile, entre les années 1850 et 1950, par exemple via le gazogène Delacotte. Il peut aussi être injecté dans un réseau de distribution gaz, ce qui était le cas au cours des années 1950, du gaz de ville, issu de la pyrolyse de la houille. À l’avenir, un gaz de synthèse issu de la gazéification de la biomasse pourrait être utilisé en remplacement du gaz naturel d’origine fossile (Lire : Biomasse et énergie : des ressources primaires aux produits énergétiques finaux). Ce gaz peut enfin être utilisé en combustion en vue de la cogénération d’électricité et de chaleur ; le rendement de conversion en électricité est amélioré, par rapport à la combustion simple de la biomasse, par l’augmentation de la température des gaz de combustion ; le rendement de conversion en électricité peut ainsi atteindre 40 % du pouvoir calorifique inférieur (PCI) de la biomasse (Lire : Co-génération et stockage saisonnier de la chaleur et Biogaz, biométhane et power-to-gas).
La synthèse de biocarburants est réalisée par gazéification du charbon en un gaz riche en CO et H2, suivi d’une synthèse Fisher-Tropsch (transformation d’un mélange CO et H2 en carburant liquide essence et diesel) ; ce procédé a été utilisé industriellement en Allemagne pendant la Seconde Guerre mondiale et, plus récemment, en Afrique du Sud (procédé SASOL) pour fabriquer des carburants liquides. Pour la biomasse, l’intérêt réside dans le fait que la gazéification permet, contrairement à la fermentation conduisant à la production d’éthanol à partir des seuls sucres de la plante, la valorisation de tous les composants de la biomasse lignocellulosique en carburants tels que le méthanol, le diméthyléther (DME) ou encore les hydrocarbures obtenus par une synthèse Fischer-Tropsch.
2. Les principes de base et les réactions chimiques
La thermodynamique est un outil précieux pour approcher les transformations thermochimiques de la biomasse (i.e. en température et en pression) en présence de différents réactifs. Même si l’équilibre thermodynamique est rarement atteint, cet outil permet de prévoir deux paramètres essentiels :
- La composition des produits de réaction vers laquelle tend la réaction,
- Les enthalpies de réaction.
La connaissance des enthalpies de réaction est indispensable pour toute intégration de la réaction dans un procédé industriel. À haute température (>1000°C) les cinétiques réactionnelles en phase gaz sont rapides et l’équilibre thermodynamique devient un bon indicateur de la composition des produits de réaction.
2.1. Les enthalpies de réaction, loi de Hess
Pour une réaction équilibrée (stoechiométrique) l’enthalpie de réaction, calculée aux conditions standards (20°C, 1 bar) est égale à la somme des enthalpies de formation des produits finaux diminuée de la somme des enthalpies de formation des réactifs de départ.
![]()
Lorsque Δ Hréaction < 0 la réaction est dite exothermique, le système cède de la chaleur, qui est récupérable.
Lorsque Δ Hréaction > 0 la réaction est dite endothermique, le système reçoit de la chaleur, qui doit être fournie.
L’enthalpie de formation en température et en pression peut être déterminée à partir de l’enthalpie de formation aux conditions standards (20°C, 1 bar); en général la connaissance de l’enthalpie de réaction aux conditions standards est suffisante pour une première approche.
2.2. Données thermodynamiques concernant la biomasse
Pour déterminer les enthalpies de réaction, il est donc nécessaire de connaître des enthalpies de formation de toutes les espèces qui interviennent dans la transformation chimique. Si l’enthalpie de formation des corps purs (O2, H2, C, entre autres) est, par définition, nulle, elle est tabulée pour la plupart des espèces (CO, CO2, CH4, H2O, notamment) et doit être déterminée pour les espèces plus complexes, comme la biomasse.
De manière étonnante, et même si les structures moléculaires sont très variables, la composition élémentaire de la biomasse sèche reste proche des rapports suivants : 6 atomes de carbone pour 9 d’hydrogène et 4 d’oxygène : C6H9O4. Ramenée à 1 atome de carbone, cette composition moyenne s’écrit : C H1,5 O 0,66
L’enthalpie standard de formation, valeur de base nécessaire pour le calcul des enthalpies de réaction, peut être déterminée à partir de la connaissance des enthalpies de combustion pour différentes biomasses. On trouve ainsi :
pour C6H9O4 : ΔHform = -800 ± 200 kJ par mole
ou, pour C H 1,5 O 0,66 : ΔHform = -133 ± 33 kJ par mole
Le bois qui vient d’être coupé en forêt présente une humidité moyenne de 50%, soit la masse d’eau sur la masse de biomasse sèche. Après six mois de séchage sous abri, cette humidité est de l’ordre de 25% , soit environ 2 H2O pour 1 C6H9O4. La densité d’une biomasse sèche peut être très variable. La densité intrinsèque (hors vides) est en général comprise entre 500 et 900 kg/m3.
2.3. Enthalpies standard de formation des principales espèces chimiques intervenant dans les réactions
Pour une approche simple et dans le but de pouvoir comparer facilement ces enthalpies, on ramène à un seul atome de carbone les enthalpies de formation des espèces carbonées (Tableau 1).
Tableau 1 : Enthalpies de formation de différentes espèces chimiques (ramenées à 1C pour les espèces carbonées)
| Espèces chimiques | Enthalpie standard de formation (kJ/mole) |
| H2 | 0 |
| O2 | 0 |
| C (graphite) | 0 |
| Carburant (CH2) | ~- 20 |
| CH3 (Propane ramené à 1C) | -42 |
| CH4 (méthane) | -74 |
| CO | -110 |
| Biomasse C H1,5 O0,66 | -130 |
| Ethanol (ramené à 1C (-276 kJ/mole pour
C2H5OH)) |
-138 |
| Méthanol (liquide) | -238 |
| H2O vapeur | -240 |
| H2O liquide | -280 |
| CO2 | -393 |
On observe qu’il faut beaucoup moins d’énergie pour passer du CO ou de la biomasse au méthane ou encore à un carburant (soit environ 50 à 100 kJ par atome de carbone) que pour passer du CO2 aux mêmes produits (soit 320 à 370 kJ par atome de carbone). Il s’agit évidemment de l’énergie minimale puisqu’elle correspond à une transformation à l’équilibre thermodynamique. Si l’on tient compte des pertes inéluctables de tout procédé, et sachant que ces pertes sont, en première approximation, proportionnelles à l’énergie mise en jeu, cette approche très simple permet, à elle seule, d’expliquer le peu d’intérêt, du point de vue énergétique, que présente le recyclage du CO2, par exemple, en méthane (CH4). La conversion du CO2 en méthanol nécessite une énergie moins importante (150 kJ/mole à l’équilibre thermodynamique), mais, en contrepartie et de manière tout à fait logique, l’énergie de combustion du méthanol (21,5 MJ/kg) est très inférieure à celle du méthane (51 MJ/kg).

La pyrolyse du bois, à la base de la fabrication du charbon de bois, correspond à une transformation du bois en produits solides (charbon de bois (graphite C)) et en différents gaz de décomposition tels que vapeur d’eau, méthane, CO, goudrons ou hydrogène. Il s’agit d’une technologie très ancienne (Figure 1) mais encore très usuelle dans les pays en développement, notamment au sud du Sahara.
La transformation de la biomasse sèche à température imposée de 700°C peut être calculée à l’équilibre thermodynamique :
C6H9O4 à 700°C => 0,27 H2O + 0,1 CH4 + 0,21 CO2 + 4,1 H2 + 3,36 CO + 2,3 C (solide) (Réaction 1).
Le bilan enthalpique donne une énergie de réaction de +270 ± 200 kJ (endothermique) pour une mole de C6H9O4 ou encore +45 ± 33 kJ pour une mole de C H 1,5 O 0,66.
La réaction est donc endothermique : il faut apporter de l’énergie pour la réaliser. Cette énergie correspond à la combustion d’une ou deux moles d’hydrogène pour la réaction 1 car l’oxygène de l’air va préférentiellement sur l’hydrogène. Si l’on tient compte des pertes thermiques des dispositifs de fabrication du charbon de bois, il est probable que l’essentiel de l’hydrogène formé et peut-être du CH4 et du CO soient consommés par combustion avec l’oxygène de l’air, pour fournir l’énergie nécessaire. De plus, la réaction réelle n’étant pas à l’équilibre thermodynamique, on produit aux températures de transformation en charbon de bois (entre 300°C et 400°C) des composés goudronnés, dits hydrocarbures aromatiques polycycliques (HAP), qui partent avec les fumées.
Il resterait donc, in fine, essentiellement 2,3 C solide pour, initialement, C6H9O4, ce qui représente environ 20% de la masse initiale de biomasse sèche. On retrouve ainsi les rendements connus des procédés de transformation du bois en charbon de bois. On notera que seulement environ 1/3 du carbone initialement présent dans le bois est transformé en charbon de bois (Figure 1). (Lire : De la découverte du feu à la combustion de la biomasse)
2.4. Pyrolyse et gazéification à haute température imposée (T>1300°C)
Les calculs thermodynamiques montrent qu’une transformation à haute température imposée (>1300°C) de biomasse sèche conduit à la réaction suivante, quelle que soit la pression dans un domaine de p < 100 bars :
C6H9O4=> 2C + 4 CO + 4,5 H2 avec : ΔH = +330 ± 200 kJ endothermique.
L’ajout de 2 moles d’eau conduit à la transformation suivante :
C6H9O4 + 2 H2O => 6 CO + 6,5 H2 avec : ΔH = +640 ± 200 kJ fortement endothermique.
Les réactions à très haute température produisent donc essentiellement les espèces gazeuses CO et H2. C’est le domaine de fonctionnement des réacteurs de gazéification à flux entraîné[1].
2.5. Pyrolyse et transformation chimique en présence d’eau à température intermédiaire et à pression imposée (500 à 900°C ; 1 et 10 bars)
C’est le domaine de fonctionnement des réacteurs de gazéification à lit fluidisé. Sachant que la pyrolyse de biomasse sèche produit, en partie, du carbone solide, on peut convertir ce carbone en gaz par la mise en œuvre, dans ce type de réacteur, de la vapeur d’eau avec un double objectif :
- convertir le carbone résiduel,
- assurer la fluidisation du lit.
Les conditions de fluidisation, soit la mise en suspension dense de particules dans un courant fluide ascendant, imposent l’utilisation d’un débit minimum de vapeur, qui se traduit par un apport équivalent, au minimum, d’environ 4 moles d’eau (H2O) pour une mole de C6H9O4 (Tableau 2).
Tableau 2 : Espèces gazeuses obtenues avec C6H9O4 (biomasse) + 4 H2O à températures intermédiaires (500 et 900°C) et à pression variable, à l’équilibre thermodynamique
| P=1 bar | P=10 bars | |||
| 500°C | 900°C | 500°C | 900°C | |
| H2 | 2,9 | 7,2 | 1,07 | 6,6 |
| CO | 0,46 | 5,3 | 0,13 | 5 |
| H2O | 3,2 | 1,3 | 3,8 | 1,6 |
| CO2 | 2,1 | 0,7 | 2 | 0,8 |
| CH4 | 1,2 | 0,03 | 1,8 | 0,2 |
| Enthalpie de réaction (kJ) aux conditions standards | +70 | +630 | 0 | +540 |
Au vu des résultats ci-dessus, il est clair que la production des espèces H2 et CO est favorisée par une augmentation de la température et que la production de méthane (CH4) l’est par les températures les plus faibles et les pressions les plus élevées. D’où les conclusions suivantes :
- si l’objectif est la cogénération, on cherchera à produire un gaz combustible riche (en termes de PCI/m3) ce qui conduira à favoriser la production de méthane ; dans ce cas, on utiliserait plutôt un procédé basse température (500 à 800 °C) mais à haute pression, typiquement réalisable en lit fluidisé ;
- si l’objectif est la fabrication de carburants de 2ème génération par synthèse Fisher-Tropsh (FT), on cherchera à privilégier la production de CO et de H2. On utilisera donc préférentiellement un procédé haute température comme les réacteurs à flux entraîné.
Si l’on cherche à produire un carburant à partir d’une synthèse FT, cette réaction peut s’approcher, de manière simplifiée par la réaction suivante: CO + 2 H2 => CH2 (chaîne carburant) + H2O (-160 kJ/mole ; exothermique). Le rapport H2/CO nécessaire pour la synthèse FT est donc bien de 2.
On constate (Tableau 2) que le rapport molaire H2/CO produit par la gazéification d’une biomasse est, à haute température, toujours sensiblement inférieur à 2. Il sera donc nécessaire d’ajuster ce rapport avant de procéder à une synthèse FT. La technique d’ajustement de ce rapport aura un impact important sur le rendement en carburant de synthèse. On constate aussi que les réactions à haute température sont beaucoup plus endothermiques et nécessitent donc un apport d’énergie plus important que les réactions à plus basse température. En contrepartie, l’énergie contenue dans les gaz de synthèse obtenus est beaucoup plus importante. Mais il n’est pas pertinent de discuter de cette énergie tant que le mode d’apport d’énergie n’aura pas été précisé.
2.6. Les techniques d’apport d’énergie
L’apport d’énergie, relatif au seul poste de gazéification, concerne l’énergie de réaction mais aussi l’énergie nécessaire pour :
- porter les réactifs à la température et à la pression désirée,
- compenser les pertes thermiques,
- injecter les réactifs dans le dispositif de gazéification.
Le principe le plus simple d’apport d’énergie consiste à brûler (oxydation par injection d’un gaz réactif comportant de l’oxygène) une partie de la biomasse et à utiliser cette énergie pour transformer, ou gazéifier car le gaz réactif contient aussi de la vapeur d’eau, l’autre partie. On parle, dans ce cas, de procédé autothermique. Cette manière de faire consomme évidemment une partie significative de la biomasse, ce qui réduit la part gazéifiée et, in fine, la production finale visée (gaz, électricité ou carburant).
Une alternative visant à transférer l’essentiel de la matière dans le produit final, ce qui est le cas des biocarburants, consiste à apporter une énergie externe. On parle alors de procédé allothermique. Dans une logique de décarbonatation de l’énergie, il faudra, bien entendu que cette énergie alternative soit décarbonée ou que le CO2 associé produit puisse être séquestré efficacement.
Les possibilités techniques d’apport d’énergie dépendent bien entendu des technologies de gazéification.
2.7. Apports d’énergie dans les lits fluidisés
Dans un lit fluidisé, l’un des problèmes est de convertir, par réaction avec la vapeur d’eau, le carbone produit par la pyrolyse de la biomasse qui a tendance à s’accumuler dans le lit car les cinétiques réactionnelles avec la phase solide sont relativement lentes. Mais on peut aussi utiliser ce carbone pour apporter l’énergie nécessaire à la gazéification. La solution autothermique consiste alors à brûler tout ou partie de ce carbone.
Si l’on injecte l’oxygène nécessaire à cette combustion directement dans le lit avec la vapeur d’eau, les calculs thermodynamiques montrent que l’oxygène aura tendance à réagir préférentiellement avec les gaz de pyrolyse, en particulier avec l’hydrogène et le méthane, et non avec le carbone solide. Pour éviter cette réaction, on peut organiser une recirculation du matériau du lit contenant le carbone vers un lit secondaire où s’effectuera la combustion du carbone solide. On parle alors de lit fluidisé recirculant. Cette solution permet aussi de séparer les gaz de pyrolyse, relâchés dans le réacteur principal, des gaz de combustion, relâchés dans le réacteur secondaire. La combustion échauffe le matériau de fluidisation qui sert alors au transfert de l’énergie vers le réacteur principal.
Dans la mesure où la combustion s’effectue dans un réacteur secondaire, on peut aussi envisager d’injecter du gaz naturel , source d’énergie fossile, dans le réacteur secondaire (principe allothermique). Il faudrait alors séquestrer le CO2 issu de la combustion.
2.8. Apports d’énergie dans les réacteurs à flux entraînés
Les réacteurs à flux entraînés fonctionnent à plus haute température (> ~1200°C). Il s’agit essentiellement d’un four circulant dans lequel on injecte la bio-ressource en même temps que les gaz réactifs (eau, …).
Le principe le plus simple d’apport d’énergie consiste, là aussi, à injecter de l’oxygène qui entraîne une combustion partielle. Les calculs thermodynamiques montrent alors que la réaction (autothermique) a tendance à être la suivante :
C6H9O4 + 2 H2O + 2,5 O2 =>~ 4,55 CO + 3 H2 +3,55 H2O + 1,45 CO2
Par rapport à une réaction sans apport d’oxygène (tableau 2), on s’aperçoit que l’oxygène réagit préférentiellement avec l’hydrogène et affecte faiblement la production de CO. La conséquence est donc que le transfert du carbone dans le gaz de synthèse reste efficace, mais le rapport molaire H2/CO est significativement réduit : il devient même sensiblement inférieur à 1 alors qu’il faut un rapport 2 pour la synthèse FT.
On peut aussi envisager un apport de gaz combustible dans le réacteur à flux entraîné, méthane (source fossile) ou hydrogène (procédé allothermique). Comme le montre l’exemple ci-dessous, il serait alors possible d’augmenter significativement le rapport molaire H2/CO (ici égal à 2) tout en conservant le nombre de moles de CO et en apportant l’énergie nécessaire à la réaction :
C6H9O4 + 5 H2O + 2,5O2 + 1,5CH4 => 4,5CO +9 H2 + 3CO2 + 3,5H2O
Dans cet exemple, la séparation suivie de la séquestration de 3 CO2 permettrait de séquestrer plus de carbone que le carbone apporté par le méthane fossile. Il existe, bien entendu, nombre de variantes possibles pour la composition des réactifs. Leur sélection dépendra de nombreux paramètres tels que,
– les choix techniques concernant le rééquilibrage du rapport H2/CO en aval du réacteur de gazéification,
– les conditions de fonctionnement du réacteur de synthèse FT : rendement, recycles des gaz n’ayant pas réagi, entre autres,
– les conditions de séparation du CO2,
– les possibilités techniques de séquestration du CO2,
– les coûts d’investissements des différents composants,
– les conditions économiques.
2.9. L’ajustement du rapport molaire H2/CO
La technique classique d’ajustement du rapport H2/CO consiste à utiliser la réaction du gaz à l’eau (Water Gas Shift) qui consiste à transformer une partie du CO produit par la gazéification en hydrogène et en CO2 :
CO + H2O gaz=> H2 + CO2 ΔH= -30 kJ
Cette réaction réduit significativement le nombre de moles de CO qui serviront à la synthèse FT, et, en conséquence, le rendement en carburant de synthèse. On peut alors remplacer cette technique par un apport externe d’hydrogène, hydrogène obtenu par électrolyse ou hydrogène de reformage de méthane donc fossile, ce qui, dans ce dernier cas, nécessiterait la séquestration du CO2. Un apport externe d’hydrogène augmente, bien entendu, le rendement en carburant de synthèse.
On retiendra que le rendement masse en carburant (masse de carburant produite rapportée à la masse de biomasse sèche en entrée) varie, en fonction des solutions retenues, entre ~15% (procédé entièrement autothermique) et ~55% (apports externes importants)2b.
3. Les procédés industriels de gazéification
Quels sont, sur la base des principes de base de la gazéification, rappelés ci-dessus, les principes de mise en œuvre industrielle, les problèmes génériques liés à cette mise en œuvre et les caractéristiques des gaz produits ?
Les dispositifs de gazéification de la biomasse sont dérivés des procédés développés pour la gazéification du charbon[1]. La plupart se classent dans les principales catégories suivantes (Figure 2) :
- Les lits fixes Co- ou contre- courant
- Les lits fluidisés
- Les lits fluidisés circulants
- Les réacteurs à flux entraîné (ou en courant fluide).
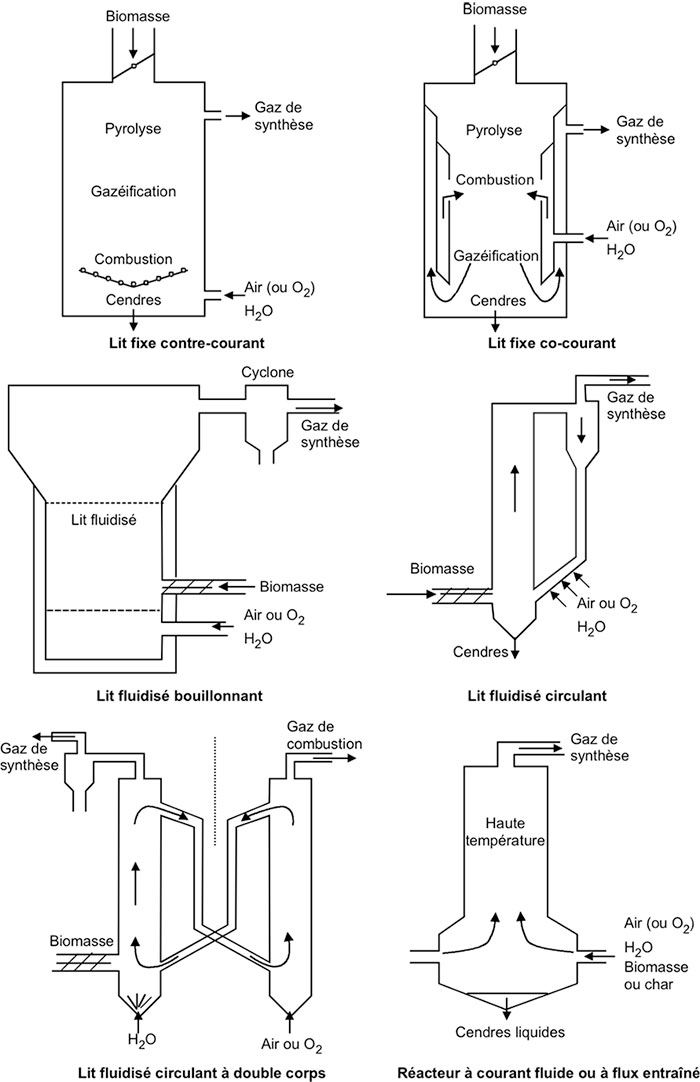
Ces divers principes de fonctionnement de réacteurs de gazéification sont à l’origine de réalisations industrielles de différents types (Tableau 3).
Tableau 3 : Récapitulatif de différentes technologies de gazéification
| Technologie de gazéification | Exemples de Gazéifieur |
| Lits fixes à contre-courant | Wellman-Galusha, Ansaldo-Volund, Bioneer |
| Lits fixes à co-courant | DTU , TKE, Biomass Engineering,
Fluidyne, De Lacotte |
| Lits fluidisés bouillonnants | EPI, Andritz-Carbona |
| Lits circulants | FICFB, Lurgi, Foster Wheeler, Leroux&Lotz |
| Lits circulants à double corps | Ferco SILVAGAS |
| Réacteurs à flux entraîné | Texaco, Prenflo, Lurgi MPG, Shell, Bioliq |
3.1. Les lits fixes à contre-courant (updraft)
Dans les lits fixes à contre-courant, le solide se déplace lentement vers le bas d’un réacteur vertical dans lequel les réactifs gazeux sont introduits par le bas. On rencontre, du bas vers le haut, tout d’abord une zone dans laquelle les réactions de combustion prédominent et la température est élevée (~1200 °C) puis une zone dans laquelle se produisent les réactions de réduction avec la production de CO et H2 et où la température diminue. Les gaz s’échappent en traversant la zone supérieure de pyrolyse. Les cendres sont évacuées en partie inférieure.
La technologie est simple, fiable et éprouvée pour des particules solides de taille uniforme et sans particules fines. Cet agencement favorise la production d’un gaz sale à basse température avec un fort taux de présence de goudrons (de l’ordre de 100 g/Nm3), ce qui limite son utilisation à la combustion. Il semblerait que ce type de technologie soit limité à des débits de biomasse sèche de l’ordre de 4 t/h (20 MWth)[3]. Le procédé Lurgi adapté à la gazéification du charbon va jusqu’à une production de 100 MWth. Les installations de pyrolyse en vue de la production de charbon de bois peuvent être assimilées à un lit fixe dans lequel l’air de réaction est introduit par le bas.
3.2. Les lits fixes à co-courant (downdraft)
Dans les lits fixes à co-courant, le solide se déplace lentement vers le bas dans un réacteur vertical où les réactifs gazeux sont introduits par le haut, et/ou latéralement, car les agencements peuvent être assez variables (Figure 3). Les réactions ont lieu, pour l’essentiel, dans une zone limitée. Les gaz de réaction quittent le réacteur par le bas à haute température.
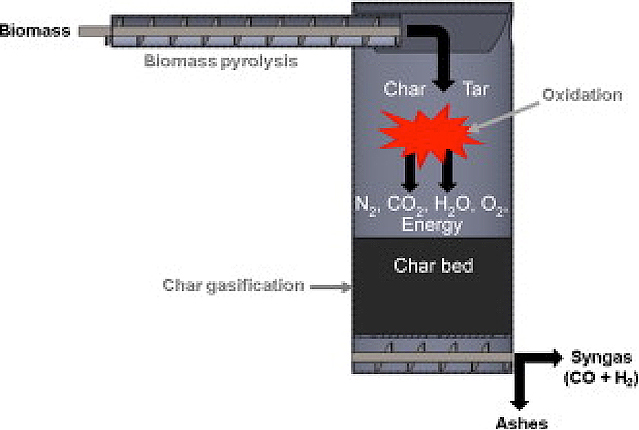
La technologie est simple, fiable et éprouvée pour des particules solides de taille à peu près uniforme d’environ 5 mm. Le gaz produit est assez propre avec une faible concentration en goudrons de quelques g/Nm3. En raison de problèmes d’instabilités tels que l’apparition de passages préférentiels d’écoulement de gaz (channelling), la technologie semble limitée, pour la biomasse, à un débit de l’ordre de 500 kg/h (2,5 MWth).
3.3. Les réacteurs à lits fluidisés bouillonnants (bubbling fluid bed)
Dans les réacteurs à lits fluidisés bouillonnants, la biomasse pré-séchée est entraînée dans un lit fluidisé par les gaz réactifs introduits en partie inférieure. Le lit fluidisé est constitué d’un matériau de fluidisation inerte (sable) ou avec effet catalytique (olivine, dolomite ou autres). Du fait de l’intensité du mélange, la température dans le lit est uniforme et facile à contrôler. La teneur du gaz produit en CO et H2 augmente avec la température du lit, qui est cependant limitée par des contraintes technologiques (matériau du réacteur) et par le risque d’agglomération du lit lié à la fusion des cendres.
En pratique, cette température ne dépasse guère 950 °C dans les applications actuelles et se situe le plus souvent autour de 700 °C à 850 °C. Les cendres sont extraites avec les particules agglomérées, ce qui nécessite un traitement et le remplacement du matériau de fluidisation. Le taux de présence de goudrons dans le gaz est moyen, de l’ordre de 10 g/Nm3. La technologie est relativement éprouvée et la limite en taille semble, pour la biomasse, se situer autour de 10 à 15 t/h (~75 MWth). Cette technologie est compatible avec un fonctionnement en pression, ce qui permet d’en diminuer la taille, donc l’investissement, et de favoriser la production de méthane (CH4).
3.4. Les lits circulants (circulating fluid bed)

Dans les lits fluidisés circulants, la biomasse pré-séchée est introduite dans un lit fluidisé circulant au sein duquel la re-circulation s’effectue par une « jambe descendante » (Figure 4). Le gaz de synthèse est séparé de l’écoulement solide en partie supérieure du réacteur. Cette technologie permet d’augmenter la vitesse de circulation, donc les cinétiques de réaction. Elle présente par ailleurs les mêmes avantages et contraintes que la technologie de lit fluidisé bouillonnant. Compte tenu de la complexité accrue, la technologie ne présenterait un intérêt économique que pour les débits de biomasse élevés (15t/h ou plus).
3.5. Les lits circulants à double corps (twin fluid beds)
La technologie des lits circulants à double corps est une extension de celle dite à lit circulant. Un système de recirculation permet d’assurer, dans le circuit de retour, le mélange du matériau de fluidisation et de charbon de bois dans un réacteur séparé dans lequel s’effectue la combustion du solide résiduel. Ce système permet de séparer les gaz de combustion des gaz de synthèse. Le matériau recirculant devient alors un caloporteur qui transfère l’énergie de combustion du carbone solide résiduel vers le réacteur de gazéification. La température dans le réacteur de gazéification se situe aux alentours de 800 °C à 900 °C comme pour les technologies lit fluidisé ou lit circulant. La température dans le réacteur de combustion ne dépasse guère 950 °C à 1000 °C pour des raisons technologiques et de risques d’agglomération.
Ce faible écart de température entre le réacteur de gazéification et le réacteur de combustion (100 °C à 150 °C) impose un débit important de recirculation du caloporteur. En pratique, le débit masse de recirculation du matériau de fluidisation sera égal à plusieurs dizaines de fois le débit de biomasse sèche. Ce type d’installation est assez complexe et ne serait viable, économiquement, que pour des débits importants (>10 t/h de biomasse).
3.6. Les réacteurs à courant fluide ou flux entraîné (entrained flow)
La matière, liquide ou solide, broyée finement (~100 µm), est injectée à vitesse élevée, en suspension dans un mélange de gaz réactifs (contenant de la vapeur d’eau, de l’oxygène ou de l’air) dans le réacteur. La zone réactionnelle (flamme) peut être portée à température élevée (1300 °C à 2000 °C). À ces niveaux de température les réactions sont très rapides, de l’ordre de quelques secondes, favorisant la formation de CO et H2 ainsi que le vaporeformage du méthane et la destruction des goudrons. Les cendres passent à l’état liquide. Une fraction des particules de cendres fondues est récupérée sur les parois du réacteur, ou peut être plus ou moins séparée du courant gazeux par séparation inertielle. Une partie du solide carboné peut être entraînée par le gaz.
Cette technologie permet de supprimer les problèmes posés par l’utilisation d’un matériau de fluidisation et de favoriser la production de CO et H2 ainsi que le reformage du méthane et la destruction des goudrons. En contrepartie, elle requiert, pour que la cinétique de réaction soit suffisamment rapide, la nécessité d’injecter la biomasse sous forme de fines particules (100 à 200 µm pour le charbon et 400 à 800 µm pour la biomasse). Ce type de réacteur implique un prétraitement coûteux de la biomasse.
Différentes préparations peuvent être envisagées.
- Préparation par pyrolyse lente. La biomasse peut être préalablement pyrolysée dans un réacteur séparé. Le gaz de pyrolyse est séparé du solide carboné résiduel (char). Ce solide carboné, broyé finement, est ensuite injecté à vitesse élevée, en suspension dans un mélange de gaz de pyrolyse et de gaz réactifs (contenant de la vapeur d’eau, de l’oxygène ou de l’air) dans le réacteur.
- Préparation par torréfaction. Le broyage très fin de la biomasse ligneuse coûte très cher en énergie. Un moyen de diminuer le coût énergétique du broyage est de rendre les particules mécaniquement fragiles. Ceci serait possible par l’intermédiaire d’une torréfaction préalable. Les recherches sont en cours dans ce domaine. Le traitement de torréfaction entraîne cependant une perte de matière et d’énergie.
- Préparation par pyrolyse rapide ou pyrolyse « flash »[4]. La biomasse est préalablement soumise à une pyrolyse par chauffage rapide à température intermédiaire (~500°C). Cette pyrolyse est suivie d’une trempe rapide des gaz de pyrolyse. Cette technique permet d’obtenir un mélange liquide (aussi appelé pétrole vert) et un solide carboné. Le solide peut aisément être broyé finement et mélangé au liquide pour obtenir un slurry. Ce dernier est pompable et peut assez facilement être injecté dans le réacteur. Ce procédé soulève cependant un certain nombre de problèmes liés à une perte de matière significative (entre 15 et 30 %) et à des problèmes de contrôle des propriétés des mélanges (risque de séparation de phases, acidité, viscosité élevée, notamment).
La technologie de réacteur à flux entraîné requiert aussi un soin particulier au niveau de la conception des parois du réacteur haute température et de celle des échangeurs de récupération de la chaleur du gaz. Cette technologie est utilisée pour la gazéification du charbon (Texaco) avec des unités de l’ordre de 80 MWth.
4. Problèmes génériques liés aux technologies de gazéification de la biomasse
Les problèmes génériques à résoudre, liés aux technologies de gazéification de la biomasse, sont de plusieurs ordres et concernent, en particulier :
- l’alimentation régulière à fort débit d’un solide dans un réacteur sous pression,
- l’obtention d’un gaz de synthèse débarrassé des goudrons et autres impuretés,
- l’agglomération des lits fluidisés due essentiellement à la teneur en cendres de la matière première,
- la corrosion des structures engendrées par la présence d’éléments minéraux dans la biomasse.
4.1. Alimentation en biomasse solide
Dans certains cas, il est intéressant de pouvoir réaliser la gazéification dans un réacteur sous pression dans la mesure où la diminution de taille entraîne une diminution significative des investissements. Par ailleurs, en réalisant la gazéification sous pression, il ne sera pas nécessaire de comprimer le gaz pour réaliser, en aval du réacteur de gazéification, les réactions d’ajustement de composition du gaz ou de synthèse de carburant, ce qui représente une économie d’énergie intéressante. Mais cela pose un problème délicat d’introduction de la biomasse solide dans le réacteur sous pression.
Les technologies existantes d’introduction du solide sont, pour la plupart, basées sur des systèmes de convoyage par vis sans fin et/ou l’utilisation de sas intermédiaires (lock hopper). Ces techniques présentent de nombreux problèmes liés aux bouchages, à l’usure, au blocage de pièces d’étanchéité, à l’introduction de gaz inertes comme l’azote, entraînant des coûts de maintenance élevés. Une manière de résoudre le problème pourrait résider dans une transformation préliminaire de la biomasse en un liquide combustible par pyrolyse flash, comme dans le procédé BIOLIQ[5] .
4.2. Génération et destruction de goudrons
Comme décrit précédemment, la gazéification produit des goudrons qui sont entraînés dans le gaz, en quantité variable selon le procédé utilisé. Par exemple, les procédés à lit fixe ou à lit fluidisé décrits auparavant produisent un gaz contenant entre 1 g/Nm3 et 100 g/Nm3 de goudrons. La tolérance aux goudrons pour les réactions de synthèse étant très faible (~0,0001 g/Nm3) il est nécessaire d’éliminer ces goudrons. Ceci représente un point clef pour les procédés de gazéification de la biomasse.
Les goudrons générés par la gazéification ont fait l’objet de très nombreuses études ; une classification a été proposée en fonction de caractéristiques réfractaires croissantes, en goudrons « primaires, secondaires et tertiaires », ainsi que des listes typiques de goudrons que l’on retrouve dans le gaz pour les différentes technologies de gazéification[6]. Lorsque la température augmente, au-dessus de 800 °C, ne subsistent pratiquement plus que des goudrons dits tertiaires, formés d’hydrocarbures monoaromatiques tels que benzène et toluène (classé parmi les composés organiques volatils (COV)) et d’hydrocarbures aromatiques polycycliques (HAP) tels que naphtalène, pyrène, phénanthrène, anthracène, entre autres. Ces espèces chimiques sont converties en gaz aux températures élevées (1300 °C à 1500 °C), l’une des plus réfractaires étant le naphtalène. Autour de 1200°C, ces espèces se transforment également en suies qui sont très réfractaires.
De très nombreux travaux ont été effectués sur les technologies de destruction des goudrons[7]. L’émission de goudrons peut être réduite en utilisant dans le réacteur de gazéification un matériau de fluidisation capable de catalyser la conversion des goudrons. Il a ainsi été montré que des matériaux naturels comme l’olivine [(Mg,Fe2)SiO4] ou la dolomite [CaMg(CO3)2] ont un effet catalytique[8]. Des catalyseurs métalliques à base de Ni ont été développés[9]. L’un des problèmes rencontrés est la désactivation du catalyseur due aux interactions avec les inorganiques contenus dans la biomasse tels que le soufre.
Ces catalyseurs peuvent également être utilisés dans des lits secondaires placés en aval du gazéifieur.
En prenant en compte ces différents éléments liés à l’utilisation de catalyseurs dans des réacteurs de gazéification dont la température de sortie est inférieure à 1000 °C, la teneur en goudrons pourrait être réduite à une valeur de l’ordre de 0,1 g/Nm3. Une élimination plus complète pourra s’effectuer après refroidissement du gaz, par lavage à basse température au niveau de l’étage de traitement du gaz.
4.3. Agglomération des lits fluidisés
Le phénomène d’agglomération des lits fluidisés est lié aux réactions physicochimiques entre les cendres et le matériau de fluidisation[10]. Les cendres contiennent des espèces ayant une basse température de fusion comme :
- des oxydes fondant entre 500 °C et 1000° C : Na2O, K2O, PbO, MnO, B2O3,
- des nitrates comme KNO3 et NaNO3, qui fondent également en dessous de 350 °C,
- des phosphates comme Cu(PO3)2 et KPO3 qui fondent entre 700 °C et 1000 °C,
- des chlorures comme NaCl et KCl qui forment un azéotrope liquide vers 650 °C alors que KCl fond vers 770 °C.
Certaines espèces, comme les oxydes et les chlorures, peuvent réagir avec le matériau de fluidisation, en général un oxyde, pour former des eutectiques ou autres composés oxydes ou oxychlorures liquides à basse température, dès 500 °C. Les composés liquides formés provoquent l’agglomération des particules de matériau de fluidisation. Il y aurait apparemment deux régimes d’agglomération:
- un régime dit homogène, à la température maximum d’environ 800 °C où les particules s’entourent de produits de décomposition des cendres, la taille des particules pouvant ainsi croître de 200 µm à quelques millimètres,
- un régime dit hétérogène, à plus haute température, entre 800 et 1000 °C où il y a création de grosses particules au sein du lit fluidisé. Ce régime se verrait auto-accéléré dans la mesure où les grosses particules entraînent l’existence de points chauds entraînant eux-mêmes une augmentation de l’agglomération.
Pour une température et une composition de cendres données, certains matériaux de fluidisation, comme la silice SiO2, formeront une masse de composés liquides plus importante que d’autres matériaux plus réfractaires et plus fragiles, comme MgO ou CaO. Ceci explique la meilleure résistance à l’agglomération de matériaux de fluidisation comme la dolomite [CaMg(CO3)2]. Dans ce cas, il ne sera pas possible d’extraire les espèces à bas point de fusion des eutectiques et autres composés formés avec le matériau de fluidisation.
4.4. Corrosion
Les problèmes de corrosion des structures métalliques existent essentiellement dans les zones de hautes températures (tuyauteries, dispositifs de filtration, échangeurs). Ils sont dus à la présence, dans la ressource comme la biomasse et donc dans le gaz de synthèse, d’espèces inorganiques volatiles, en particulier des chlorures (NaCl, KCl, HCl), des sulfures (H2S) et quelques métaux (Na, K, Hg…)[11]. Les mécanismes de corrosion sont complexes et dépendent de très nombreux paramètres, en particulier de la pression et de la température locale. Le développement d’aciers spéciaux résistants est un enjeu technologique important pour le fonctionnement des gazéifieurs.
4.5. Traitement des gaz
La biomasse renferme de nombreux éléments autres que C, H et O (Tableau 4). Même si leur concentration est faible, de l’ordre de 1 % masse dans le bois, ces éléments représentent une charge importante à éliminer, puisqu’elle peut représenter jusqu’à 500 kg/h pour une usine traitant 50 t/h de bois. Cette élimination est rendue complexe par l’étendue du spectre des éléments présents et leur importante variabilité en fonction de la nature de la biomasse utilisée. Dans un gazéifieur, ces éléments vont se recombiner chimiquement entre eux ainsi qu’avec l’hydrogène, l’oxygène et le carbone, pour se retrouver sous différentes formes telles que des carbonates et des oxydes réfractaires.
Les espèces mineures gazeuses dominantes dans le gaz de synthèse réducteur sont H2S et HCl, mais on trouvera aussi des espèces comme ZnS, NaCl, KCl, qui peuvent condenser au-dessus de 400 °C et provoquer des phénomènes de corrosion, comme peuvent le faire, à pression élevée, certaines espèces chlorées. Ces espèces solides, gazeuses ou condensables, seront éliminées par la mise en place de dispositifs assez complexes de nettoyage du gaz[12].
Tableau 4 : Concentrations typiques d’espèces mineures dans la biomasse
| Espèces et éléments | Masse par kg de biomasse sèche | Elément | Masse par kg de biomasse sèche | Elément | Masse par kg de biomasse sèche |
| Cendres
(CaCO3, SiO2) |
~ 10 g |
||||
| N | ~ 1 g | Ba | ~ 14 mg | Na | 10 à 50 mg |
| S | ~ 0,1 g | Cr | ~ 5 mg | Ni | ~ 5 mg |
| Cl | 50 à 100 mg | Fe | ~ 50 mg | P | ~ 100 mg |
| F | ~ 3 mg | K | 0,5 à 1 g | Pb | ~ 1 mg |
| Al | ~ 50 mg | Mg | ~ 0,5 g | Sb | ~ 50 mg |
| As | ~ 1 mg | Mn | ~ 50 mg | Zn | ~5 mg |
5. Unités de démonstration existantes et besoins en recherche et développement
Il existe, au niveau industriel, des procédés de production de carburants par gazéification du charbon, comme avec Sasol en Afrique du Sud. Les réacteurs de gazéification de la biomasse ont, jusqu’à présent, été essentiellement développés pour des applications en cogénération : Varnamo, Batelle, FICFB, PRME, entre autres. Toutefois, certaines installations visaient déjà la production de carburants, comme l’unité de démonstration ASCAB, de Clamecy en France, qui a fonctionné vers la fin des années 1980. La baisse des prix du pétrole, survenue à cette époque, avait alors entraîné le ralentissement, sinon l’arrêt de ces projets. Les développements ont repris depuis quelques années, en en Allemagne notamment, mais ces projets n’ont pas encore atteint le stade de maturité industrielle.
Les besoins en recherche et développement pour l’industrialisation des procédés de gazéification de la biomasse en vue de la fabrication de biocarburants apparaissent donc indispensables. Ils relèvent aussi bien de la recherche de base, de la recherche technologique, de l’intégration du procédé ou bien encore de l’évaluation technico-économique et environnementale :
– recherches de base : cinétiques réactionnelles à haute température et pressions variables : reformage du méthane, destruction des goudrons, gazéification du résidu carboné, comportement des espèces inorganiques (condensation, corrosion, aérosols, purification des gaz) ;
– recherches technologiques : technologie de préparation de la biomasse (pyrolyse rapide, torréfaction), alimentation par un solide d’un réacteur sous pression, comportement des parois de réacteur à haute température[13], filtration des gaz, échangeurs haute température, matériaux résistant à la corrosion ;
– intégration procédé : intégration énergétique, optimisation de l’utilisation des produits de la synthèse autres que les carburants (combustion, recirculation vers le reformage) ;
– évaluations technico-économiques : optimisation de la chaîne de production, possibilité de décentralisation (pyrolyse), synergies locales (utilisation de la chaleur, notamment).
Conclusion
Les technologies de gazéification de la biomasse sont très proches des technologies industrielles déjà mises en œuvre pour le charbon ou pour le reformage du gaz naturel. La biomasse pose cependant des problèmes spécifiques liés à la collecte, à la préparation, au traitement des espèces inorganiques. (Lire : Bioénergies : les chaînes d’approvisionnement de la biomasse, éléments clef de leur développement). Pour la biomasse, différentes briques technologiques existent pour la mise en œuvre d’un procédé autothermique, mais il manque l’expérience industrielle de fonctionnement d’un procédé intégré.
L’intérêt de cette technologie réside dans le fait qu’elle ouvre de nombreuses options procédés qui permettent d’adapter la même technologie à différentes ressources telles que le charbon (Carbon to Liquid -CTL), les pétroles lourds, la biomasse (Biomass to Liquid-BTL), le gaz naturel (Gaz to Liquid-GTL), voire les déchets organiques, tout en permettant d’envisager l’utilisation de divers appoints (électricité, hydrogène, gaz naturel) pouvant augmenter significativement le rendement de production de carburant de synthèse. Par ailleurs, différents types de carburants peuvent être produits : diméthyléther, gazole, kérosène, méthanol, et même hydrogène.
Finalement, les procédés évolués permettraient de stocker électricité et hydrogène, issus des énergies renouvelables intermittentes, dans un carburant liquide qui ne poserait pas de problème de stockage ou de distribution et ne nécessiterait pas de modifications des moteurs actuels.
Notes et références
[1] On verra plus loin sous quelle forme l’énergie nécessaire pourra être apportée dans un réacteur réel.
[2] Loison (1983)
2b Seiler et al. (2010)
[3] MWth désigne la puissance thermique des installations (PCI de la ressource multiplié par le débit masse).
[4] Raffelt et al., 2004
[5] Daumen et al., 2012 ; Bridgewater et al., 1996.
[6] Milne et al., 1998.
[7] Sutton et al., 2001.
[8] Donnot et al., 1994.
[9] Rapagna et al., 2002.
[10] Lin et al., 1999 et Olofsson et al., 2002.
[11] Baker, 2004.
[12] Boerrigter et al., 2004.
[13] Coda et al., 2007 et Froment et al., 2015.
Bibliographie complémentaire
Donnot A, Magne P, Deglise X, (1991). Experimental approach to the catalyzed cracking reaction of tar from wood pyrolysis. Journal of Analytical and Applied Physics, 21, pp 265-280.
Froment K., Seiler J.M., Poirier J., Colombel L.,( 2015). Determining cooling screen slagging reactor operating temperature, Energy Fuels, 29 5077-5089
Lin W, Dam-Johansen K, (1999). Agglomeration in fluidised bed combustion of biomass – Mechanisms and co-firing with coal. Proc. 15th international conference of Fluidized Bed Combustion. Savannah, Georgia. May 16-19.
Loison R., (1983). Gazéification du charbon. Les techniques de l’ingénieur. J 5 410.
Milne TA, Abatzoglou N, Evans RJ, (1998). Biomass Gasifier «Tars»: Their Nature, Formation, and Conversion. NREL/TP-570-25357.
Olofsson G, Ye Z, Bjerle I, Anderson A, (2002). Bed Agglomeration Problems in Fluidized Bed Biomass Combustion. Industrial and Engineering Chemistry Research, 41 (12).
Raffelt K. et al., (2004). Stable slurries from Biomass pyrolysis products for entrained flow gasification 2nd World conference on Biomass for energy. Industry and Climate Protection, 10-14 May 2004, Rome
Rapagna S, Provendier H, Petit C, Kiennemann A, Foscolo PU, (2002). Development of catalysts suitable for hydrogen or syn-gas production from biomass gasification. Biomass and Bioenergy, 22 pp 377-388., Italy.
Seiler J.M., Hohwiller C., Imbach J., Luciani J.F. Technical and economical evaluation of enhanced biomass to liquid fuel processes Energy 35 (2010) 3587-3592
Sutton D, Kelleher B, Ross JRH, (2001). Review of literature on catalysts for biomass gasification. Fuel Processing Technology, 73, pp 155-173.
Références concernant les technologies de gazéification:
Andritz-Carbona :https://www.andritz.com/products-en/group/pulp-and-paper/power-generation/gasification/bfb-gasifiers
Ansaldo Volund : www.volund.dk/
Bioliq: https://www.bioliq.de/english/67.php
Biomass Engineering: http://gasifiers.bioenergylists.org/gasifiers/biomass-engineering-ltd-0
Bioneer: http://gasifier.bioenergylists.org/content/finnish-bioneer-gasifiers
DTU http://sol3d.com/_backup/1.0/publications/lg/gasifier.pdf
FICFB : Rauch et al. (2004) “Steam gasification of biomass at CHP Plant in Guessing –Status of the Demonstration Plant” 2nd World Conference and Technology Exhibition on Biomass for Energy, Industry and Climate Protection, 10-14th May 2004, Rome, Italy
Fluidyne : http://www.fluidynenz.250x.com.
Foster Wheeler: https://link.springer.com/chapter/10.1007/978-3-642-02682-9_6
MPG: Liebner W., Ulber D. (2004) Lurgi Multipurpose Gasification; Gasification Technologies Conference San Francisco, California October 8-11, 2000 Biomass Gasification Overview DOE/NREL January.
Prenflo: https://www.globalsyngas.org/uploads/eventLibrary/28RADTKE.pdf
Shell: Rob van den Berg 2017, An integrated solution for efficient coal-to-products value chains Gasification India Conference New Delhi, India Copyright of Shell Global Solutions International B.V.December 06-07
Silvagas: M.A. Paisleya, J.M. Irvingb, R.P.Overendc A promising power option – the Ferco Silvagas Biomass gasification process; operating experience at the Burlington gasifier.
B Burlington Electric Department, National Renewable Energy Laboratory, Burlington, VT 05401
Texaco : Texaco Gasification Process: US Environmental Protection Agency, EPA 540/R-94
TKE : https://www.sciencedirect.com/topics/engineering/fixed-bed-gasifiers
Wellman-Galusha : https://www.researchgate.net/figure/Wellman-Galusha-fixed-bed-gasifier-showing-gravity-coal-feed-system-18_fig14_255200911
L’Encyclopédie de l’Energie est publiée par l’Association des Encyclopédies de l’Environnement et de l’Énergie (www.a3e.fr), contractuellement liée à l’université Grenoble Alpes et à Grenoble INP, et parrainée par l’Académie des sciences.
Pour citer cet article, merci de mentionner le nom de l’auteur, le titre de l’article et son URL sur le site de l’Encyclopédie de l’Energie.
Les articles de l’Encyclopédie de l’Energie sont mis à disposition selon les termes de la licence Creative Commons Attribution – Pas d’Utilisation Commerciale – Pas de Modification 4.0 International.





