Peut-on améliorer le bilan carbone de la production-utilisation de l’hydrogène ? De nombreuses technologies devraient le permettre, de la photo-électrolyse aux micro-organismes photosynthétiques. Qui sont les auteurs de ces avancées potentielles ? Où en sont-ils de leurs recherches ?
Intéressant du point de vue énergétique, l’hydrogène présentait jusqu’à récemment d’importantes contraintes de transport[1]. Toutefois, les avancées sur le stockage solide permettent d’espérer une accélération de son développement. En outre, ce vecteur énergétique propose une valorisation des énergies renouvelables, dans un contexte de meilleure intégration au réseau électrique, ainsi qu’une redéfinition de l’intégration territoriale des systèmes énergétiques[2].
L’hydrogène ne figure pas au rang des énergies vertes, puisque les procédés actuels de production utilisent majoritairement des hydrocarbures (gaz naturel, pétrole, charbon). Dans une perspective de remplacement des énergies fossiles par l’hydrogène, cette dépendance doit être reconsidérée en vue d’une refonte complète de l’industrie de production d’hydrogène.
Bien que les technologies de captage et stockage du CO2,voire de son utilisation, permettent aux procédés actuels de considérablement diminuer les empreintes environnementales[3], il est crucial de se concentrer sur les procédés de production d’hydrogène n’émettant aucun gaz à effet de serre et ayant recours à des énergies renouvelables. Ajoutons enfin qu’il est usuel de parler d’hydrogène produit, ce qui est un abus de langage, puisque les procédés permettent la production de dihydrogène (H2). Toutefois, pour plus de simplicité, c’est le terme d’hydrogène qui sera utilisé dans ce qui suit.
1. Production et utilisation de l’hydrogène en 2014-2015
Les récentes avancées dans le stockage solide ou la valorisation des énergies renouvelables démontrent une forte activité de recherche dans la technologie hydrogène ainsi qu’une réduction des coûts. Ces évolutions ne reflètent toutefois pas les tendances actuelles de production et de consommation.
1.1. Principales filières de production
L’hydrogène produit au cours de l’année 2014 provient à 96% de procédés utilisant des hydrocarbures et à 4% de l’électrolyse (Tableau 1). Cependant, ces données considèrent aussi la coproduction ; l’émission d’hydrogène non volontaire lors du raffinage (via les hydrocarbures liquides), la production de coke (via le charbon dans la sidérurgie), la production de dichlore et d’hydroxyde de sodium (via l’électrolyse). Finalement, seul 10% de l’utilisation de l’électrolyse de l’eau a pour objectif la production d’hydrogène[4].
Parmi les procédés développés en vue d’une production d’hydrogène, le reformage du gaz naturel est actuellement le plus utilisé. Les principaux producteurs mondiaux en 2014 étaient Air Products (18,5 milliards de mètres cubes), Air Liquide (13 milliards de mètres cubes), Praxair, et Linde. De plus, la plus grande partie de la production se fait actuellement au sein de réseaux internes aux sites industriels recourant à l’hydrogène[5].
Tableau 1 : Origine de l’hydrogène produit (coproduction incluse).
| Origine de l’hydrogène | Pourcentage |
| Gaz naturel | 49% |
| Hydrocarbures liquides | 29% |
| Charbon | 18% |
| Électrolyse | 4% |
Source : AFHYPAC.
1.2. Utilisations de l’hydrogène
Deux grandes familles d’usages doivent être distinguées ; l’hydrogène énergie et l’hydrogène pour l’industrie. Même si la recherche actuelle porte principalement sur la première utilisation, avec comme objectif d’obtenir un nouveau vecteur énergétique[6] pour le stockage d’électricité, le power-to-gas [7]ou la mobilité, les applications pratiques dans l’industrie restent majoritaires. Au sein de ces dernières, l’hydrogène est principalement valorisé en tant que matière première.
Il constitue ainsi un élément essentiel dans différents procédés chimiques (Tableau 2). Le premier poste de consommation est la fabrication d’ammoniac, composant de base dans l’industrie des engrais[8]. Si, en comparaison avec cet usage, la fabrication d’autres produits chimiques est minoritaire (amines, méthanol, eau oxygénée), son utilisation dans l’élaboration de matériaux (métaux, verres), la soudure ou l’industrie alimentaire tend à augmenter[9].
En outre, près de 44% de la consommation mondiale d’hydrogène (Tableau 2) est le fait de l’industrie pétrolière. Le respect des normes environnementales y requiert de grandes quantités d’hydrogène, notamment lors du procédé de désulfuration. Contenu dans les combustibles fossiles, le soufre se transforme en oxyde de soufre lors de leur combustion[10]. Il appartient donc aux acteurs du raffinage de retirer ce soufre en amont de la combustion. L’extraction et le raffinage d’hydrocarbures fournissent ainsi l’énergie nécessaire à la production d’hydrogène, permettant finalement un meilleur raffinage d’hydrocarbures.
Tableau 2 : Consommation industrielle de l’hydrogène
| Monde (2013) | Union européenne (2006) | France (2008) | |
| Raffinage du pétrole | 44% | 47% | 59% |
| Ammoniac, engrais | 38% | 39% | 26% |
| Chimie de base (dont méthanol) | 8% | 8% | 10% |
| Métallurgie | – | 6% | 1% |
| Divers | 10% | – | 4% |
| Total (en milliers de tonnes par an) | 60 000 | 8 250 | 922 |
Source : Actualité chimique n°347, Alphea, France Stratégie, 2014
Face à ces utilisations industrielles, l’utilisation de l’hydrogène comme vecteur d’énergie ne représente que 1% de la consommation, concentrée dans la propulsion d’engins spatiaux, tels que les satellites ou les fusées. La consommation dans les piles à combustible n’en représente qu’une infime part, malgré une croissance de leur production de près de 400% entre 2008 et 2013[11].
2. Le bilan carbone de l’hydrogène
Selon l’origine de l’énergie utilisée pour la production d’hydrogène, le bilan carbone est plus ou moins élevé. Le procédé le plus largement répandu, le vapore formage du méthane, présente un bilan carbone excédentaire, avec 10 kg de dioxyde de carbone (CO2) par kilogramme d’hydrogène produit. La teneur élevée en CO2 des gaz émis par ce procédé permet cependant la mise en place de systèmes de captage et stockage du CO2[12]. À l’inverse, l’utilisation d’énergie électrique d’origine renouvelable permet d’obtenir une empreinte carbone nulle au procédé de fabrication de la source et des composants, donc un hydrogène que l’on qualifie de « vert ». Les fortes émissions de gaz à effet de serre des procédés de production actuels expliquent le faible intérêt des véhicules à hydrogène en termes de réduction des émissions[13].
La production d’hydrogène représente environ 3% des émissions totales de gaz à effet de serre (GES) au niveau mondial, et près de 11 millions de tonnes de CO2émises annuellement en France. Ce faible pourcentage caractérise toutefois une utilisation industrielle[14] faible en quantité consommée en comparaison avec une future utilisation de masse à des fins de stockage (avec restitution sous plusieurs formes : électricité oupower-to-gas) ou de mobilité. L’émergence de procédés de production décarbonés économiquement viables constitue donc un enjeu environnemental crucial pour un accès de l’hydrogène au rang des énergies vertes de masse. L’opportunité en termes de réduction des émissions de GES devient décisive si l’on inclut dans cette perspective la part du transport, à hauteur de 27,6% des émissions en France en 2013 dont 92% pour le seul transport routier[15].
3. Les technologies de production d’hydrogène « vert »
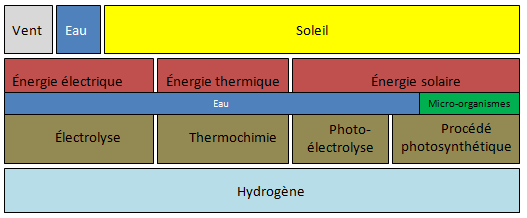
Relativement rare à l’état moléculaire dans la nature, l’hydrogène est un composant de base de nombre d’éléments : eau, déchets organiques, hydrocarbures et autres. Sa production nécessite donc une décomposition moléculaire, réalisable selon différents procédés : électrolytique, thermochimique, photo-électrolytique, biochimique. Dans ce qui suit, de ce document, seules les technologies permettant la production d’un hydrogène totalement « vert » seront considérées.
3.1. L’électrolyse
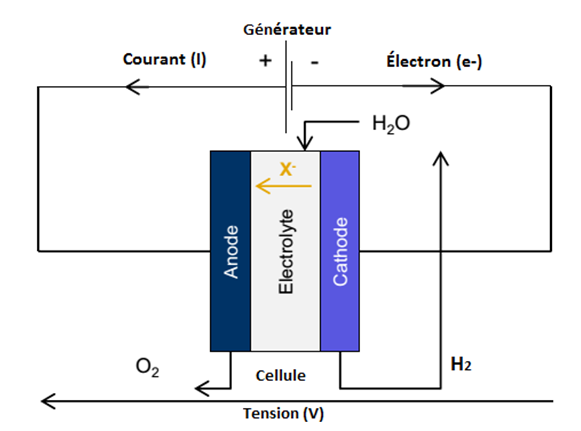
Ce procédé transforme l’énergie électrique en énergie de décomposition moléculaire, via une réaction d’oxydo-réduction. La cellule permettant cette séparation est constituée d’une anode, d’une cathode et d’un électrolyte (substance conductrice ionique). La réaction d’oxydation se produisant à l’anode permet de récupérer de l’oxygène, et la réaction de réduction se produisant à la cathode permet de récupérer de l’hydrogène. Finalement, la réaction de décomposition s’écrit :
$$ H20+énergie électrique rightarrow H2+frac{1}{2}[0]_{2}+chaleur$$
3.1.1. Description du système
Les cellules sont disposées en série électrique au sein des technologies actuelles, grâce à des électrodes bipolaires (anode d’un côté et cathode de l’autre), permettant une meilleure compacité et une densité de courant plus élevée. Ce dernier point constitue un aspect important dans le fonctionnement nominal d’un électrolyseur. En effet, le taux de production d’hydrogène de la cellule augmente avec la tension aux bornes des cellules (d’une valeur minimale de 1,23V pour engager la réaction), tandis que l’efficacité des cellules diminue. Le producteur doit ainsi effectuer un compromis entre ces deux critères.
Les cellules sont ensuite organisées en assemblages communément appelés stacks[16], puis couplées à différents appareils permettant d’obtenir les conditions optimales en eau et électricité en entrée (redresseur, osmoseur inverse, réservoir) ainsi que de stocker l’hydrogène en sortie (compresseur, réservoir). De plus, le procédé d’électrolyse étant exothermique, un dispositif d’élimination de la chaleur produite est aussi installé. Cet ensemble forme l’électrolyseur.
3.1.2. Rendement et consommation du système
Dépendant de la tension électrique et du compromis effectué par le producteur avec le taux de production d’hydrogène, les rendements des électrolyseurs actuels s’étalent de 62% à 89% selon les technologies et les conditions, notamment celles de l’eau en entrée[17].
Ainsi, 4 à 5 kWh et 1 litre d’eau sont consommés par normo-mètre cube produit dans les électrolyseurs industriels[18]. Finalement, la production d’un kilogramme d’hydrogène, permettant un déplacement de 100 kilomètres pour tout véhicule léger à pile à combustible, nécessite de 44 à 55 kWh d’électricité et 11 litres d’eau.
L’électrolyse constitue le procédé de production d’hydrogène décarboné le plus mature technologiquement. Toutefois, il ne contribue actuellement qu’à 1% de la production volontaire d’hydrogène du fait d’un manque d’investissements et de coûts dissuasifs.
3.1.3. Les différentes technologies
Il existe à ce jour trois types d’électrolyse dont la maturation va de la recherche en laboratoire à la commercialisation. Leur principale différence réside dans l’électrolyte utilisé. Quelles en sont les principales caractéristiques et le possible couplage avec des systèmes de production à bases d’énergies renouvelables ?
- L’électrolyse alcaline
Cette première technologie utilise une solution d’hydroxyde de potassium (KOH) comme électrolyte[19]. L’électrolyse alcaline constitue la solution de production d’hydrogène la plus utilisée de nos jours, et propose un coût d’investissement faible en comparaison avec les autres technologies d’électrolyse, notamment grâce à la simplicité des matériaux.
Bénéficiant déjà de rendements de 68 à 77%, l’électrolyse alcaline possède une marge d’amélioration limitée et une faible réactivité aux variations de puissance. Si ce dernier aspect est problématique pour un couplage avec des énergies intermittentes, il présente peu d’inconvénients pour la production d’hydrogène à partir de l’hydroélectricité.
Les perspectives d’amélioration de cette technologie se situent au niveau des coûts de fabrication, de la pression de fonctionnement et des conditions de couplage aux énergies intermittentes. Elle pourrait aussi profiter à terme de la recherche sur les piles à combustible alcalines[20]. Ces améliorations sont cependant minimes au vu de sa maturité, si bien que la recherche se focalise sur les deux autres technologies d’électrolyse dont les perspectives d’amélioration des performances sont plus grandes.
- L’électrolyse PEM (Proton Exchange Membrane)
Une seconde technologie d’électrolyseur utilise une membrane en polymère (PEM pour Proton Exchange Membrane) comme électrolyte. Cette évolution d’un électrolyte liquide à un électrolyte solide permet de considérablement réduire les coûts de maintenance, d’entretien, dus aux effets de l’électrolyte liquide sur l’installation, ainsi que de compression de l’hydrogène en sortie. De plus, l’électrolyse PEM propose une excellente solution de production décentralisée, grâce à une meilleure réactivité aux variations de puissance ainsi qu’une grande compacité du système[21].
Avec des rendements de 62 à 77%, cette technologie est utilisée dans certains marchés de niche, notamment dans les sous-marins, mais elle reste encore en phase de développement pour une utilisation de masse. Le recours à des matériaux nobles, notamment le platine, la durée de vie des membranes ainsi que les limitations de taille des assemblages constituent les principaux obstacles rencontrés.
Les coûts actuels des électrolyseurs PEM sont de l’ordre du double de ceux des technologies alcalines. Toutefois, cette technologie profite de la forte recherche sur les piles à combustible PEM[22], et dispose de caractéristiques prometteuses (forte densité de courant acceptée, pression élevée). Les perspectives d’amélioration identifiées se situent principalement au niveau de la capacité des empilements, de la diminution de l’utilisation des matériaux nobles ainsi que d’une augmentation de la durée de vie des membranes. Enfin, la recherche en laboratoire expérimente cette technologie à haute température (130-180°C, contre 70 à 80°C pour les électrolyseurs actuels).
- L’électrolyse à haute température
L’augmentation de la température lors d’une réaction d’électrolyse permet un apport d’énergie supplémentaire sans que l’énergie nécessaire à la décomposition moléculaire augmente[23]. Cela conduit à la suppression de catalyseurs nobles (platine ou iridium) ainsi que l’énergie électrique à fournir pour atteindre le seuil de décomposition, ce qui diminue fortement les coûts d’investissement et de fonctionnement.
La principale technologie d’électrolyse à haute température est la cellule d’électrolyse à oxyde solide (SOEC pour Solid Oxide Electrolysis Cell). Fonctionnant entre 700 et 900°C, l’électrolyse SOEC présente un dispositif similaire à l’électrolyse PEM[24]. Cependant, une part significative de l’énergie est apportée sous forme de chaleur, qui passe de 10% à 400 Kelvin à 30 % à 1200 Kelvin, mais qu’il est possible de récupérer lors de l’électrolyse (exothermique). Cette technologie présente l’avantage de pouvoir fonctionner de manière réversible : en électrolyseur ou en pile à combustible[25].
Avec des rendements pouvant dépasser 90%, l’électrolyse SOEC se situe dans la phase de recherche en laboratoire. Si les rendements actuels sont prometteurs, la dégradation accélérée des cellules constitue le principal frein à un développement rapide.
3.1.4. Évolution des coûts
Au delà des facteurs propres à chaque technologie, la diminution des coûts dans l’optique d’un développement de masse de l’électrolyse s’appuie sur des aspects communs aux différents électrolyseurs. Ainsi, afin d’optimiser l’utilisation des dispositifs de conversion d’électricité ou de purification de l’eau, il est nécessaire d’augmenter la puissance disponible par une mise en parallèle d’un plus grand nombre de stacks par électrolyseur[26].
D’autre part, une réduction des coûts nécessite à la fois un accroissement de la capacité de production par installation, via une amélioration de la capacité des cellules, ainsi que la mise en place d’une production en série.
À la différence des systèmes procédant à une conversion directe de l’énergie comme la photo-électrolyse de l’eau, une part du coût de l’électrolyse provient des installations de raccordement au réseau ou à une source de production d’électricité. Le coût de production de l’hydrogène par électrolyse dépend donc majoritairement de l’investissement initial ainsi que du coût de l’électricité utilisée.
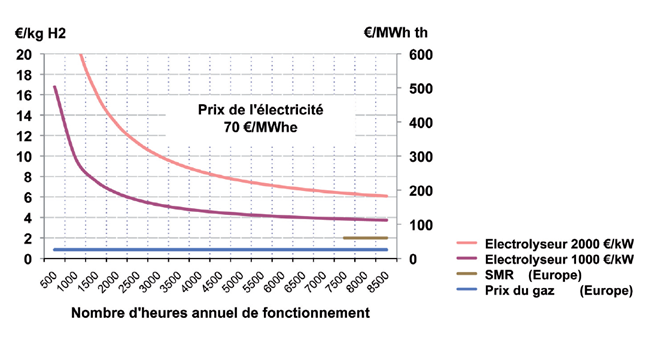
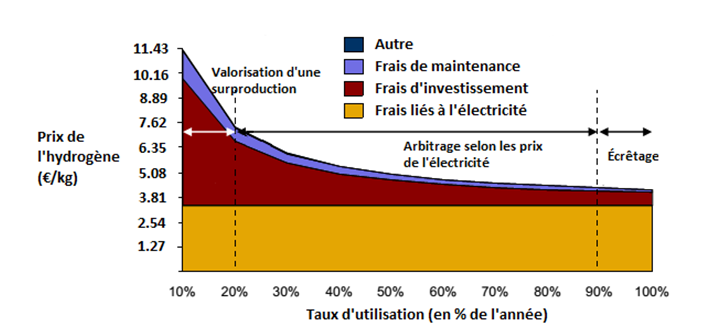
Un des enjeux majeurs en vue de rendre ce procédé économiquement viable est donc d’atteindre un coût de l’électricité d’origine renouvelable concurrentiel avec le prix du gaz utilisé pour le reformage. L’amélioration des électrolyseurs (rendement, matériaux diminuant la maintenance) constitue un autre facteur décisif, auquel s’ajoute la nécessité de la mise en place d’une production d’électrolyseurs en série afin de diminuer leur part dans le coût d’investissement. Enfin, une augmentation du nombre d’heures de fonctionnement permet de réduire la part représentée par l’investissement, et finalement le coût de l’hydrogène. La Figure 3 illustre l’évolution du coût du kilogramme d’hydrogène en fonction de ces différents facteurs, et la Figure 4 permet d’en observer la part du coût final[27].
Si la plupart des estimations situent entre 2 et 4 euros le prix du kilogramme d’hydrogène produit par électrolyse à horizon 2020, les études américaines semblent plus optimistes. Compte-tenu de la forte corrélation entre le prix de l’hydrogène par électrolyse et le prix de l’électricité, les politiques énergétiques, ainsi que la part des énergies renouvelables dans le mix électrique, jouent un rôle primordial dans les prévisions effectuées. Les prévisions de France Stratégie sont corroborées par les données de l’U.S.DRIVE, annonçant des prix de l’ordre de 3,80 euros en 2015, diminuant à 2,25 euros le kilogramme en 2020 pour une installation de petite taille[28].
3.2. La photo-électrolyse de l’eau
Ce procédé de conversion directe de l’énergie solaire en énergie chimique permet une production d’hydrogène « vert » décentralisée. Il s’appuie sur les technologies développées dans l’industrie des panneaux photovoltaïques.
3.2.1. Le procédé et ses avantages
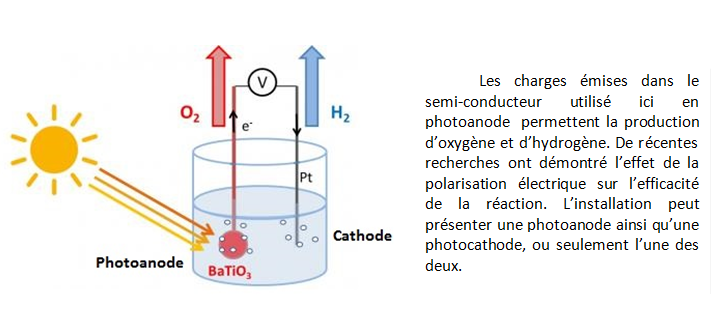
L’utilisation de semi-conducteurs comme photo-catalyseurs au sein d’un électrolyte aqueux permet de capter les photons afin de fournir l’énergie nécessaire à la migration des électrons de la bande de valence à la bande de conduction au sein du matériau semi-conducteur. Cette illumination aboutit à la réaction des électrons avec l’eau à la surface des photo-catalyseurs[29], dissociant l’eau en oxygène et hydrogène (voir Figure 5).
L’intérêt majeur de ce procédé réside dans la conversion directe de l’énergie solaire, évitant ainsi tout coût d’installation électrique ou de raccordement au réseau. De plus, contrairement aux procédés utilisant l’énergie thermique, la photo-électrolyse s’effectue à faible température[30], diminuant les contraintes sur les installations. Ces aspects positifs, ainsi que sa forte parenté avec les technologies solaires, en font une solution possédant un fort potentiel de développement.
En 2013, le département de l’Énergie des États-Unis annonçait des rendements de 12,4% à 18,3% ce que l’on peut comparer au rendement d’un assemblage photopiles (15%) et d’un électrolyseur (75%), soit au total un rendement de l’ordre de 12%. Toutefois, des physiciens du Laboratoire nano-magnétisme et oxydes du CNRS ont récemment annoncé avoir doublé l’efficacité du procédé d’électrolyse via la polarisation électrique[31].
3.2.2. Les obstacles
Encore au stade de développement, la recherche se focalise sur l’amélioration des performances des matériaux semi-conducteurs utilisés ainsi que sur la compréhension des phénomènes, notamment la durée de vie des trous électroniques. En effet, ceux-ci représentent une part significative du coût du dispositif et n’atteignent pas les performances nécessaires à une viabilité économique du procédé, particulièrement en termes d’absorption lumineuse, de durée de vie et de coût. Par exemple, l’activité de l’un des photo-catalyseurs le plus utilisé, le dioxyde de titane, est limitée à 4% du spectre solaire[32]. Ensuite, les semi-conducteurs doivent être protégés, en raison de la corrosion induite par les électrolytes aqueux utilisés[33].
Ces contraintes augmentent la part déjà élevée du capital dans le coût total imputable aux semi-conducteurs. En effet, si la simplicité du procédé réduit les coûts d’investissement et de maintenance, les matériaux actuellement utilisés pour les électrodes ne permettent pas d’aboutir à un prix de production de l’hydrogène concurrentiel.
3.2.3. Évolution des coûts
Le département de l’Énergie des États-Unis annonçait en 2013 un coût de production de l’hydrogène d’environ 13,1 euros par kilogramme d’hydrogène pour l’année 2015, ainsi qu’une cible de 4,3 euros pour 2020.
Toutefois, un groupe de chercheurs appartenant à l’École polytechnique fédérale de Lausanne ainsi qu’à l’université Technion (Israël) a développé des semi-conducteurs à base d’oxyde de fer. Les coûts annoncés s’élèvent à seulement 5 euros par kilogramme[34], avec des rendements compris entre 1,4% et 3,6%. Cette avancée, ainsi que l’utilisation de la polarisation électrique, concrétisent la dynamique de la recherche afin de diminuer les coûts et d’augmenter les rendements.
3.3. La dissociation thermochimique de l’eau
Cette technologie apporte l’énergie de décomposition sous forme thermique à l’aide d’installations solaires thermodynamiques à concentration ou de centrales nucléaires à haute température[35]. Toutefois, la température nécessaire pour atteindre une décomposition spontanée est considérable[36].
3.3.1. Le procédé et ses avantages
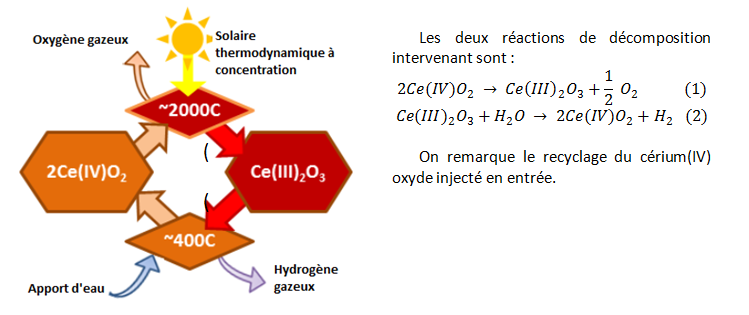
Afin de diminuer l’énergie dépensée pour atteindre cette température, d’augmenter la durée de vie des matériaux, réduite à haute température, et de faciliter leur fabrication, le procédé de dissociation thermochimique a recours à des substances chimiques[37]. La succession de réactions intervenant entre elles, ainsi qu’avec l’eau, permet finalement d’obtenir la décomposition de l’eau en oxygène et hydrogène à des températures réduites d’environ 700°C. Ce procédé fonctionne selon des cycles chimiques, dans lesquels l’énergie thermique permet à la fois les réactions nécessaires à l’obtention de l’hydrogène mais aussi celles aboutissant au recyclage des substances introduites. Cette technologie propose donc une solution de production d’hydrogène propre, consommant uniquement de l’eau et de la chaleur provenant de sources solaires ou nucléaires.
3.3.2. Les obstacles
La dissociation thermochimique de l’eau se situe en début de développement et présente une forte dépendance aux avancées des technologies solaires à concentration dont les cycles actuels les plus prometteurs ont des rendements de l’ordre de20%[38]. Si le potentiel de cette technologie est considérable, de nombreux freins ont été identifiés par le Sandia National Laboratories (département de l’Énergie des États-Unis) :
- la faible connaissance des cycles thermochimiques utilisés constitue un frein à l’amélioration des rendements ainsi qu’à une diminution des coûts liés à la multiplication des réactions ;
- Le degré de technicité exigée est élevé aux températures atteintes ; les défis concernent à la fois la durée de vie des matériaux face aux températures d’utilisation et aux substances corrosives, la fabrication du réacteur, sa gestion en fonctionnement (chaleur, séparation au sein de certaines réactions chimiques) ainsi que les technologies de solaire concentré qui nécessitent des progrès ;
- la surface au sol nécessaire à l’implantation de telles installations ainsi que leur degré de technicité entraînent un coût d’investissement élevé.
3.3.3. Évolution des coûts
Le département de l’Énergie des États-Unis a mené une étude d’évolution des coûts de l’hydrogène en fonction de différents facteurs[39]. La simulation se base sur une centrale solaire thermodynamique à concentration de 13km² possédant une capacité de production de 100 tonnes d’hydrogène par jour (Tableau 3).
Tableau 3 : Synthèse étude Département de l’Énergie
| Facteurs | Rendement | Durée de vie des matériaux | Baisse du coût du réacteur | Coût du solaire concentré | Coût en $/kg | Coût en €/kg |
| 2015 | 6,2% | 1 an | – | 140$/m² | 35,22 | 27,1 |
| 2020 | 16,7% | 5 ans | 30% par rapport à 2015 | 75$/m² | 8,56 | 6,6 |
| Au-delà | 34,3% | 10 ans | 30% par rapport à 2020 | – | 3,84 |
2,95 |
Chacun de ces facteurs a aussi un potentiel de diminution de coût dont il ressort que le rendement de la dissociation thermochimique de l’eau constitue l’élément le plus décisif. Son augmentation de 6,2% à 34,3% permet de réduire le coût du kilogramme d’hydrogène de plus de 87%.
3.4. L’utilisation de micro-organismes photosynthétiques
La dernière voie de production d’hydrogène « vert » imite un procédé se déroulant dans la nature. En effet, certains micro-organismes produisent naturellement de l’hydrogène par photosynthèse.
3.4.1. Le procédé et ses avantages
Cette technologie exploite les capacités photosynthétiques d’algues vertes ou de cyanobactéries pour produire de l’oxygène et de l’hydrogène. Les photons solaires sont d’abord captés par un pigment contenu dans les organismes, la chlorophylle, puis permettent de produire deux enzymes[40]. La chlorophylle perd alors des électrons, remplacés par d’autres lors d’une photolyse de l’eau.
La différence du procédé visant à produire de l’hydrogène intervient dans une seconde phase, au cours de laquelle le dioxyde de carbone réduit, afin de produire les glucides nécessaires au développement de l’organisme, est remplacé par des protons. La réaction de réduction provoquée permet de produire de l’hydrogène moléculaire.
L’eau et le soleil constituent les deux seules sources d’énergie de ce procédé. Il autorise donc une production d’hydrogène en dissociation complète avec les infrastructures actuelles. De plus, l’absence de recours à des électrodes ou à des semi-conducteurs permet d’éliminer toute contrainte sur la qualité de l’eau ce qui diminue le coût des dispositifs habituellement couplés et offre plus de possibilités d’implantation.
3.4.2. Les obstacles
À l’aube de son développement en 2016, ce procédé nécessite une meilleure compréhension des phénomènes chimiques afin d’optimiser les organismes. Par exemple, au cours de la seconde phase, l’enzyme hydrogénase catalyse la réduction finale des protons, transformant les ions H+ en molécules d’hydrogène. Cependant, l’oxygène inhibe le fonctionnement de cette enzyme. Coproduit avec l’hydrogène lors de ce procédé, il limite la durée de production d’hydrogène à quelques minutes au maximum. Un axe de recherche consiste donc à bloquer les effets de l’oxygène en modifiant la structure de l’enzyme[41]. D’autre part, la production combinée d’oxygène et d’hydrogène constitue un second obstacle, puisqu’un dispositif supplémentaire est nécessaire. Enfin, l’efficacité de cette technologie est naturellement limitée par l’énergie solaire maximale absorbable par les organismes. Ces derniers n’utilisent qu’une faible partie de l’énergie théoriquement disponible et dissipent le reste sous forme de chaleur[42].
3.4.3. Évolution des coûts
La dissociation thermochimique de l’eau n’étant qu’au tout début de son développement, il existe peu d’estimation de coût de l’hydrogène produit. Pour sa part, le département de l’Énergie des États-Unis estime un coût du kilogramme produit d’environ 6,9 euros en 2020, avec un rendement du procédé supérieur à 5%.
4. Projets et acteurs de la filière hydrogène décarboné
Le développement technologique et industriel des procédés évoqués ci-dessus s’accompagne de l’élaboration d’une stratégie d’intégration de l’hydrogène au sein des réseaux énergétiques. De nombreuses initiatives visent à étudier cette intégration, afin d’en observer les verrous et de progressivement convaincre de sa viabilité.
4.1. Recherche et pôles de compétitivité
La recherche française en matière d’hydrogène se structure principalement autour de deux entités : le groupe de recherche HYSPAC du CNRS – Hydrogène, systèmes et piles à combustible, regroupant plus d’une centaine d’équipe ainsi que de nombreux industriels – ainsi que le CEA. En plus des systèmes de production d’hydrogène, la recherche française adopte une approche verticale, en étudiant les matériaux utilisés, notamment au sein du Laboratoire des interfaces et surfaces d’oxydes (LISO) et du Laboratoire d’électrochimie et de physicochimie des matériaux et des interfaces (LEPMI). En parallèle de cette recherche technologique, un institut de recherche sur la sûreté industrielle – l’INERIS – contribue à la prévention des risques, et une agence publique – l’ADEME – oriente la recherche via des projets ou investissements. Au niveau mondial, les acteurs sont évidemment beaucoup plus nombreux.
En interaction entre le monde de la recherche et les projets industriels, deux pôles de compétitivité interviennent dans le domaine de l’hydrogène : Capenergies et Tenerrdis. Au sein de ce dernier, 48 projets liés à l’hydrogène énergie ont été financés par l’État ou les collectivités territoriales depuis 2005, dont 24% dans la production d’hydrogène[43].
4.2. Projets et entreprises
Parallèlement à une recherche active sur l’amélioration des procédés, de nombreux projets sont conduits sur la filière hydrogène dans sa globalité ainsi que sur la viabilité de son intégration dans les réseaux énergétiques. Ils sont illustrés par les quatre exemples suivants.
4.2.1. Un projet français terminé : Horizon Hydrogène Énergie
Une initiative publique de grande ampleur appelée Horizon Hydrogène Énergie (H2E) a été lancée en 2008[44]. Ce projet a été cofinancé par l’État, et coordonné par Air Liquide, pour une durée de sept ans[45]. Il a rassemblé 17 partenaires (entreprises, instituts, laboratoires) dont deux intervenants sur la phase de production d’hydrogène : Areva Stockage d’Énergie (électrolyseurs PEM) et le CEA. Parmi les projets lancés, le projet MYRTE s’est focalisé sur le couplage avec les énergies renouvelables[46]. Il a étudié un couplage entre des panneaux photovoltaïques, un électrolyseur, deux installations de stockage (solide et sous pression) et une pile à combustible afin de tester la viabilité de l’écrêtage par stockage hydrogène. Il pourrait aussi contribuer au stockage d’énergie sur sites isolés.
4.2.2. Exemples d’entreprises : WH2, Atawey, Areva et McPhy
Parmi les petites et moyennes industries (PMI) rattachées au groupe de recherche HYSPAC, l’entreprise WH2, créée en 2011, propose une solution de production à partir de l’hydroélectricité. Cette PMI participe au projet PUSHY (Potentiel Use of Solid Hydrogen), qui regroupe des PMI, des industriels et un centre de recherche afin de proposer une solution hydrogène complète, de la production à l’acheminement chez le client. Ce projet se décline en deux offres, selon le lieu d’installation et l’électricité utilisée lors de l’électrolyse, avec un électrolyseur et un système de stockage solide. L’offre OSSHY (On site Solid Hydrogen) propose une production sur le site d’industriels utilisant de l’hydrogène en tant que matière première, tandis que l’offre LASHY (Local Alternative Solid Hydrogen) propose une production à partir d’énergies renouvelables, utilisée selon un arbitrage entre une valorisation en électricité ou en hydrogène.
À la centrale hydraulique de Port-Mort, sur la Seine, WH2 développe l’offre LASHY à partir d’un barrage hydroélectrique et d’une source d’eau extérieure au fleuve. L’entreprise annonce une production annuelle de 7 tonnes au cours de la période d’expérimentation qui débute courant 2016 puis 21 tonnes. L’hydrogène peut ensuite être acheminé vers le site de consommation par voie routière ou fluviale. Si les usages de l’hydrogène produit restent classiques (réseau de gaz ou mobilité), la réalisation propose une source d’approvisionnement électrique nouvelle et prometteuse. En effet, la France constitue le second pays européen producteur d’hydroélectricité avec plus de 2000 petites centrales au fil de l’eau, soit 8500 MWe installés[47]. L’un des objectifs de l’expérimentation consiste donc à convaincre les exploitants de ces centrales de la viabilité technique, économique et environnementale, d’un couplage avec un système hydrogène, le principal obstacle restant néanmoins celui des coûts de production affichés : l’hydrogène produit à la centrale de Port-Mort consomme 63 kWh par kilogramme produit, soit un coût d’environ deux fois celui du gazole à environ 15 euros/kg.
Plusieurs autres entreprises développent des produits sur le marché de l’hydrogène. Dans le domaine de la mobilité, la société Atawey propose des solutions de bornes de recharge plug & play destinées à la fois aux vélos, aux voitures ainsi qu’à des engins industriels[48]. Cette solution se décline en une offre autonome, avec production d’hydrogène sur site, et en une offre approvisionnée de manière externe. Dans le domaine de la production et du stockage industriels, Areva conçoit des systèmes hydrogène sous la forme de groupes de secours à pile à combustible, d’électrolyseurs ou de groupes permettant la production d’hydrogène, son stockage puis sa restitution sous forme d’électricité. Enfin, McPhy constitue un autre exemple d’entreprise développant une forte présence sur le marché de l’hydrogène. Cette société conçoit des électrolyseurs alcalins, des solutions complètes de production, stockage et distribution d’hydrogène. De plus, McPhy est l’un des précurseurs dans le domaine du stockage solide de l’hydrogène à l’aide de galettes à base d’hydrures de magnésium[49].
4.2.3. Un projet européen en cours : Don Quichote (Demonstration Of New QUalitative Innovative Concept of Hydrogen Out of wind Turbin Electricity)
Un projet européen appelé Don Quichote propose de démontrer la viabilité de l’intégration de l’hydrogène dans un schéma énergétique renouvelable global. Un regroupement de 11 partenaires industriels et institutionnels développe depuis octobre 2012 un dispositif regroupant un électrolyseur, un compresseur et une pile à combustible. Couplé en amont à des éoliennes ainsi qu’à des panneaux photovoltaïques, il alimente en aval une flotte de véhicules à hydrogène. L’objectif consiste donc à simuler le comportement d’un réseau hydrogène de petite échelle, afin d’en valider la maturité technique et économique[50].
Ce projet est devenu pleinement opérationnel en février 2014pour sa phase 1, soit un fonctionnement en trois phases successives d’amélioration des systèmes utilisés. Ainsi, l’électrolyseur actuel de type alcalin atteint un rendement de 69%, et démarre une ou deux fois par jour car le projet fonctionne à la manière d’un réseau intelligent, au sein duquel le degré d’utilisation du parc de chariots élévateurs à hydrogène conditionne l’utilisation de l’électrolyseur. La quantité d’hydrogène produite se situe entre 41 kg et 153 kg par mois, l’électrolyseur alcalin révélant des limitations quant à l’énergie électrique nécessaire à cette production, de l’ordre de 100 kWh/kg. Ce type d’électrolyseur présentant une faible réactivité aux variations de puissance, un délai de 30 minutes est nécessaire avant d’atteindre la production nominale. Novatrice, cette expérimentation permet donc de soulever les problèmes de l’intégration d’un système hydrogène, afin de mener des études de résolutions à travers les futures améliorations: électrolyseur PEM, pile à combustible PEM, compresseur électrochimique.
4.2.4. Structure de financement de projets : Partenariat public/privé FCH JU
Le Fuel Cells and Hydrogen Joint Undertaking (FCH JU) est un partenariat à l’échelle européenne entre la Commission européenne, Hydrogen Europe (représentant 80 industriels) et le groupe de recherche N.ERGHY (regroupant 59 laboratoires et instituts). Cette concentration d’acteurs privés et publics permet d’agir à la fois au niveau de la stratégie d’intégration des technologies, du déploiement industriel ainsi que de la recherche. Après une première phase convaincante (2008-2014), le Conseil de l’Union européenne a renouvelé le partenariat pour une seconde phase, de 2014 à 2020, la dotant d’un budget de 1,33 milliards d’euros[51].
Cette initiative européenne s’organise autour de deux pôles : transport et énergie. Elle procède alors, selon les orientations de développement décidées au sein des pôles, à des appels à projets afin de stimuler les innovations ou l’amélioration des technologies. Un appel à projets structuré autour de 24 sujets a ainsi été lancé en janvier 2016, représentant un investissement de 117,5 millions d’euros. Au sein de ce troisième appel, 11 projets appartiennent au pôle énergie[52]. On y trouve par exemple le développement de procédés de production d’hydrogène à partir de l’énergie solaire ou d’un électrolyseur de grande capacité possédant un temps de réponse faible.
5. Avenir de l’hydrogène « vert »
La combinaison d’une production d’hydrogène par des combustibles fossiles et d’une consommation assurée pour moitié par l’industrie du raffinage renforce le potentiel du cycle vertueux initié par une diminution de l’utilisation d’hydrocarbures dans le mix énergétique. Cela permet alors, en plus des bienfaits environnementaux, d’augmenter la disponibilité de l’hydrogène en tant que vecteur énergétique. Le développement d’une importante capacité de production décarbonée, tant au niveau de l’électricité que du procédé de production d’hydrogène, constitue cependant l’aspect décisif. En effet, dans l’hypothèse d’une utilisation purement énergétique de l’hydrogène, la production actuelle d’hydrogène, soit 60 millions de tonnes en 2014, ne représenterait que 1,3% de la consommation mondiale d’énergie.
5.1. Évolution de la production et de la réglementation
À partir de simulations de l’évolution du marché de l’hydrogène aux horizons 2020 et 2050, quatre axes stratégiques pour le développement de la filière en France ont été identifiés[53] :
- Convergence hydrogène/énergies renouvelables,
- Électro-mobilité de nouvelle génération,
- Piles et hydrogène au service de la ville durable,
- Hydrogène et piles, vecteurs de la croissance internationale,
- Mesures transversales d’accompagnement de la filière.
Le premier axe se concentre sur un couplage de la production d’énergie renouvelable et de l’hydrogène. L’ADEME prévoit un surplus d’électricité renouvelable de 30 à 90 TWhà horizon 2050, mais il n’existe actuellement pas de capacité de stockage suffisante pour valoriser cette production. L’hydrogène pourrait constituer une réponse à ce besoin, soit un premier objectif de production d’hydrogène « vert » de 3 tonnes par heure à horizon 2020.
À l’horizon plus lointain de 2050, les visions possibles du marché de l’hydrogène sont portées par le développement des usages industriels et la volonté de construire des systèmes énergétiques peu carbonés.
Les premières sont les moins incertaines puisque l’injection d’hydrogène directement dans le réseau de gaz naturel permet d’éviter le coût de nouvelles infrastructures, mais elles nécessitent un accompagnement de la part des industriels consommateurs d’hydrogène[54].
Les secondes, axées sur une intégration locale de l’hydrogène, sont plus ambitieuses et semées de nombreux verrous car, outre la maturité des technologies concernées, l’intégration des systèmes hydrogène au sein des réseaux énergétiques en place constitue un défi de taille. Elle passe par une « gestion sociétale » et une « volonté politique forte, tant au niveau national que local »[55].
En 2016, les réglementations françaises en matière d’hydrogène s’inscrivent dans une utilisation industrielle -matière première ce qui ne facilite pas l’émergence de l’hydrogène- énergie, surtout sous une forme décentralisée[56]. Toutefois, de récentes avancées réglementaires favorisent le stockage de l’électricité par hydrogène décarboné [57].
Article 121 de la Loi relative à la transition énergétique pour la croissance verte en vigueur au 25 mars 2016 :
|
Dans un délai de douze mois à compter de la promulgation de la présente loi, le Gouvernement remet au Parlement un plan de développement du stockage des énergies renouvelables par hydrogène décarboné qui porte notamment sur :
|
5.2. Simulation d’utilisation dans la mobilité
Les perspectives d’évolution de la mobilité impliquent un fort développement des moyens de production d’hydrogène tant à l’échelle nationale que mondiale. Dans le cas de la France, différents niveaux de dépendance du parc automobile à l’hydrogène basé majoritairement sur une production par électrolyse peuvent être simulés[58]. Sur la base d’un parc automobile de 31,8 millions de véhicules particuliers au 1er janvier 2015, effectuant un trajet moyen de 12 753 kilomètres par an en 2014, les résultats suivants sont obtenus (Tableau 4)[59].
Tableau 4 : Simulation de consommation de la production d’hydrogène pour la mobilité
| Pourcentage du parc | 10% | 25% | 50% | 100% |
| Production d’hydrogène (en milliards de kilogrammes) | 0.4 | 1.01 | 2.02 | 4.04 |
| Coût d’investissement (en milliards d’euros)[60] | 14.4 | 36 | 72 | 144 |
| Électricité requise (en TWh) | 18 | 45 | 90 | 180 |
| Pourcentage de la production d’électricité française | 3.34 | 8.35 | 16.7 | 33.4 |
| Eau requise (en millions de mètres cubes) | 4.4 | 11 | 22 | 44 |
| Pourcentage de la consommation d’eau française | 0.013 | 0.033 | 0.066 | 0.13 |
Si la France se déplaçait au moyen de véhicules alimentés en hydrogène « vert », près d’un tiers de la production d’électricité serait nécessaire à cet usage, ce qui plaide pour une diversification des techniques de production (énergie thermique, solaire) si l’on veut éviter une surcharge du réseau électrique, surtout si d’autres usages de l’hydrogène se développent. En outre, les coûts d’investissement pour la seule production d’hydrogène dédiée à la mobilité sont très élevés[61].
Conclusion
La filière hydrogène actuelle est mature, mais limitée. En effet, les moyens de production par hydrocarbures sont majoritairement associés aux réseaux de sites industriels, au sein desquels l’hydrogène est valorisé sous forme de matière première. Toutefois, ce marché ne répond pas à l’émergence attendue d’un nouveau vecteur énergétique, tant en termes de capacité de production que de faibles impacts environnementaux.
Le développement d’une filière hydrogène verte nécessite de nouveaux procédés couplés à des sources d’électricité renouvelables. Parmi celles-ci, l’électrolyse présente le niveau d’avancement le plus intéressant et bénéficie du dynamisme de la recherche en termes de piles à combustible. Son extension rencontre cependant plusieurs handicaps : le coût encore prohibitif de l’hydrogène produit et la capacité de production limitée des systèmes actuels[62].
D’autres procédés démontrent une grande flexibilité par rapport aux conditions d’entrée, tant en ce qui concerne les sources d’énergie que les qualités d’eau. Cette diversité est l’un des atouts de l’hydrogène, puisque elle permet une approche double,centralisée et décentralisée, selon la proximité du réseau électrique ou le taux d’ensoleillement. Une démultiplication de la production pourrait être possible qui permettrait, à terme, d’espérer une réduction de la dépendance énergétique extérieure[63].
Le développement de la filière hydrogène ouvre aussi la voie à une reconsidération de l’intégration des énergies renouvelables en repoussant deux de leurs plus importantes contraintes : le stockage et le transport. Ce couplage propose un cycle vertueux : une augmentation de la capacité de production d’hydrogène permet de valoriser un plus grand surplus d’électricité renouvelable, l’augmentation de ce dernier justifiant des investissements croissants dans la filière hydrogène. En 2016, si la viabilité technique de certaines technologies est démontrée, la viabilité économique du modèle reste à prouver, ce qui est l’un des principaux enjeux des nombreux projets en cours et programmés.
Notes et références
[1]Voir Thierry Alleau. L’hydrogène, Encyclopedie-energie.org.
[2] Voir FinerGreen Insight, numéro 2, 2015.
[3] Voir Jean-Marie Martin-Amouroux, Captage et Stockage du CO2. Encyclopedie-energie.org. Les procédés sont le reformage du gaz naturel, la gazéification du charbon ou de la biomasse, ainsi que la fermentation (voir aussi dark fermentation, sans dépendance avec l’oxygène).
[4] Pour plus d’informations sur les procédés actuels, voir Société Chimique de France et Fiche 3.1.1 : Production d’hydrogène à partir des énergies fossiles, AFHYPAC, 2014.
[5] 88% en 2011 selon une étude du SBC Energy Institute, 2014, page 13. Voir aussi Fiche 1.3 : Production et consommation d’hydrogène aujourd’hui, AFHYPAC, 2015.
[6] Synonyme d’énergie secondaire (par exemple l’électricité ou l’essence), obtenue par conversion d’une énergie primaire (disponible dans l’environnement : eau, pétrole, vent).
[7] Voir http://www.mcphy.com/fr/marches/power-to-gas/
[8]Pour une description des procédés, voir la Société Chimique de France, données sur l’hydrogène, 2014.
[9]Voir fiche 1.3 : Production et consommation d’hydrogène aujourd’hui – AFHYPAC, 2015.
[10] Celui-ci est responsable de maladies respiratoires. Voir une illustration sur Planète Énergies.
[11] Voir Agence Internationale de l’Énergie, Technology roadmap – Hydrogen and fuel cells, 2015, page 30.
[12] Assortie de plusieurs difficultés : techniques et économiques(augmentation des coûts). Voir fiche 3.1.2 : Captage et stockage géologique du CO2 – AFHYPAC, 2014. Possibilité future d’utiliser le CO2?
[13] Voir Air Liquide, sur les performances environnementales de la voiture à hydrogène, 2008.
[14] Seules quelques milliers de personnes ont un lien avec la filière hydrogène en France selon McPhy. Voir http://www.mcphy.com/fr/hydrogene-vert/hydrogene-decarbone/
[15]http://www.developpement-durable.gouv.fr/Transports,34304.html
[16] Regroupant jusqu’à une centaine de cellules. Leur nombre est limité par des contraintes de fabrication et de tension. Pour plus de détails sur le système, voir l’étude du SBC Energy Institute, 2014.
[17]Voir la fiche 3.2.1 : Production d’hydrogène par électrolyse de l’eau – AFHYPAC, 2015.
[18] L’énergie consommée correspondant à la différence entre les énergies de décomposition et de recomposition des molécules. Un normo-mètres cube (Nm3) correspond à un mètre cube de gaz aux conditions normales de pression et de température. Un normo-mètre cube d’hydrogène contient environ 90grammes d’hydrogène.
[19] C’est la seule technologie utilisant un électrolyte liquide.
[20] Voir la fiche 3.2.1 : Production d’hydrogène par électrolyse de l’eau – AFHYPAC, 2015.
[21] Pour plus d’informations sur son fonctionnement, consulter l’étude de France Stratégie : Y a-t-il une place pour l’hydrogène dans la transition énergétique. La compacité atteinte est jusqu’à 30 fois supérieure à celle des électrolyseurs alcalins.
[22] La plus utilisée pour la mobilité, par exemple sur la Toyota Mirai.
[23] Voir Quentin Cacciuttolo. Apport de la pression sur les performances d’une cellule d´électrolyse de la vapeur d’eau à haute température. Chimie théorique et/ou physique. Université Pierre et Marie Curie – Paris VI, 2014. Français.
[24] Avec cependant un électrolyte conduisant des ions O2- à la place d’ions H+. Pour observer les schémas des dispositifs, se reporter à l’étude du SBC Energy Institute, 2014.
[25] L’électrolyse PEM aussi mais avec des performances insuffisantes. De plus, l’électrolyse SOEC permet aussi la coélectrolyse de l’eau et du dioxyde de carbone afin de produire un carburant appelé « syngas ». Cette technologie pourrait donc utiliser le CO2 stocké pour la mobilité.
[26]Le pourcentage du coût d’investissement de l’ensemble de ces dispositifs passe ainsi de 45% pour un empilement à 35% pour 50 empilements.
[27]Étude du SBC Energy Instituteen 2014 d’une centrale de 85MW, avec une durée de vie estimée à 30 ans, un coût d’investissement de 563€/kWh et un rendement de 79%. Le prix de l’électricité est fixé à 50€/MWh. Voir p59.
Sur la Figure 3, SMR signifie SteamMethane Reforming (Reformage du méthane).
[28]Sur la base de 1 euro=1,3 US $. Voir l’étude Hydrogen Production Technical Team Roadmap, 2013.
[29] Catalyseur dont l’activité est déterminée par son exposition à un rayonnement lumineux. Source : CNRTL.
[30]De 20°C à 60°C. Source : Hydrogen Production Technical Team Roadmap, 2013.
[31] Voir : Un champ électrique interne pour booster la production d’hydrogène lors de la photoélectrolyse de l’eau , CNRS, 2015
[32]Pour plus de détails sur les recherches actuelles, voir : Une nouvelle classe de photocatalyseurs activés par la lumière visible , ainsi que De la rouille, du soleil et de l’eau pour produire de l’hydrogène , CNRS, 2015.
[33]Un système d’enrobage des électrodes a été mis au point par Hypersolar. Cela permet en outre d’effectuer les procédés sans contraintes de puretés de l’eau (eau de mer, eaux usées)
[34]Highly efficient water splitting by a dual-absorber tandem cell, publiédans la revue Nature, 2012.
[35] Voir solaire thermodynamique à concentration, Connaissance des énergies.
De nouveaux réacteurs nucléaires à très haute température pourraient être consacrés à la cogénération d’électricité et d’hydrogène, par un cycle iode/soufre de dissociation thermochimique de l’eau.
[36]Plus de 3000 Kelvin pour une réaction irréversible. Voir fiche 3.2.2 : Production d’hydrogène par dissociation thermochimique de l’eau – AFHYPAC, 2016.
[37] De nombreux cycles sont possibles. Une étude du Département de l’Énergie américain (DOE) se concentre sur les 9 cycles les plus prometteurs, parmi plus de 350 disponibles. Le couple qui a été le plus étudié est le couple iode-soufre. Toutefois ce mode de fabrication est aujourd’hui en voie d’abandon.
[38]Rapport de l’énergie contenue dans l’hydrogène produit sur l’énergie solaire consommée. Ce résultat est lié au taux de conversion de l’énergie thermique en énergie chimique, dépendant du cycle thermochimique utilisé. Pour plus de détails, voir Hydrogen Production Technical Team Roadmap, 2013. Un recensement des efficacités des différents cycles est disponible ici. Pour une meilleure compréhension des chiffres, se reporter à la table de conversion du DOE.
[39]Solar Hydrogen Production with a Metal Oxide Based Thermochemical Cycle, Anthony McDaniel et Ivan Ermanoski, 2013.
[40] L’ATP et le NADPH. Le mécanisme de la photosynthèse est détaillé ici.
[41]Voir fiche 3.3.2 : Production de biohydrogène par des microorganismes photosynthétiques – AFHYPAC, 2014.
[42]Hydrogen Production Technical Team Roadmap, 2013.
[43] Pour un montant de 76 millions d’euros, voir Tenerrdis, hydrogène énergie.
[44]Site internet d’Horizon Hydrogène Énergie.
[45]Air liquide prévoit de produire la moitié de son hydrogène à partir de sources renouvelables.
[47]L’hydroélectricité : les chiffres en France et dans le monde, 2009.
[48] Karel Hubert. Stockage d’énergies renouvelables sous forme d’hydrogène pour sites isolés. Encyclopedie-energie.org
[49] Benoit Amiot. Stockage de l’hydrogène solide. Encyclopedie-energie.org
[50]Voir le site internet du projet. Le dispositif décrit ici constitue le dispositif final, après plusieurs phases d’évolution. Initialement, un électrolyseur alcalin était utilisé. Afin d’obtenir plus de détails, se reporter au compte-rendu intermédiaire de l’expérimentation, septembre 2015.
[51]Site internet du FCH JU et détails de cette seconde phase au sein du plan d’action 2014-2020.
[52]Pour un investissement de 56 millions d’euros. La liste de l’appel est disponible dans AnnualWork Plan and Budget, FCH, 2016.
[53]L’hydrogène et les piles à combustible, ADEME, 2011.
[54] L’AFHYPAC propose la mise en place de garanties d’origine hydrogène renouvelable.
[55] Voir L’hydrogène et les piles à combustible, ADEME, 2011.
[56] Voir le rapport L’hydrogène en France, AFHYPAC, 2015, page 12.
[57] Voir le projet de texte réglementaire du 22/09/2015.
[58] On considère ici une consommation de 11 litres d’eau et 44,5 kWh par kilogramme d’hydrogène produit, puis une consommation d’un kilogramme pour 100 kilomètres parcourus.
[59] Voir Comité des constructeurs français d’automobiles et INSEE, 2014.
[60] En ne considérant que l’électrolyseur (800 €/kWh espérés en 2020, selon CGSP).
[61] Hors stockage, transport, et distribution.
[62] En rapide amélioration. Voir par exemple l’installation d’électrolyse de 6MW installée à Mayence (Allemagne) par Siemens.
[63] Les importations d’énergie représentaient 70% du déficit commercial de la France sur le 1er semestre 2015.
L’Encyclopédie de l’Énergie est publiée par l’Association des Encyclopédies de l’Environnement et de l’Énergie (www.a3e.fr), contractuellement liée à l’université Grenoble Alpes et à Grenoble INP, et parrainée par l’Académie des sciences.
Pour citer cet article, merci de mentionner le nom de l’auteur, le titre de l’article et son URL sur le site de l’Encyclopédie de l’Énergie.
Les articles de l’Encyclopédie de l’Énergie sont mis à disposition selon les termes de la licence Creative Commons Attribution – Pas d’Utilisation Commerciale – Pas de Modification 4.0 International.