Marcher, manger, s’éclairer, se déplacer… tout est énergie, mais pourquoi et comment mesurer ces énergies … et en quelles unités ? La lecture de textes sur les sources d’énergie est souvent rendue difficile par la multiplicité des unités utilisées. L’éclairage de cette question est donc primordial.
Il est toujours possible de se limiter à une unité et à ses multiples pour quantifier une grandeur physique. Par exemple, le temps est exprimé grâce à la seconde, unité fondamentale, ou l’un de ses multiples comme l’heure, le jour ou l’année. Cette quantification est comprise et partagée par l’ensemble de l’humanité.
Néanmoins, de nombreuses unités dites dérivées se substituent parfois à ces unités de références, ce qui peut entrainer des confusions, des difficultés de compréhension et des problèmes de conversion. Pour la distance, le mètre, symbole m, est la référence internationale dans tous les domaines scientifiques et techniques et dans le système international d’unités (SI)[1]. Néanmoins, le mile correspondant à 1609m est largement utilisé dans les pays de langue anglaise en lieu et place du kilomètre, tout comme le pouce (équivalent à 2,54cm) ou le pied (30,48cm).
1. Le problème de l’hétérogénéité des unités énergétiques
Pour pouvoir quantifier de l’énergie, c’est encore plus nébuleux. Lors du débat national sur la transition énergétique en 2013, des personnes du public avaient exprimé la demande de limiter la communication des valeurs à une seule unité, ce qui, en dépit du caractère très légitime de la requête, n’a pas été exaucé. Le poids de l’habitude dans chacun des domaines de l’énergie est une raison de ce conservatisme, l’autre étant que l’énergie n’est pas perçue aussi directement que la distance ou le temps. Il s’agit en effet d’un concept abstrait qui s’applique à différents phénomènes concrets comme la chaleur, l’électricité, un effort physique. La définition générique de l’énergie est la propriété d’un système matériel qui se conserve au cours de transformations de ce système. Or, il existe de nombreux systèmes matériels dans lesquels ce concept d’énergie est présent, et il a fallu du temps pour concevoir une unité dans cette diversité. Par exemple, la relation entre la chaleur dégagée par un feu et le travail utilisé pour soulever une masse n’a été élucidée qu’au 19ème siècle, avec la thermodynamique (Lire : Une brève histoire de l’énergie). Nos multiples unités d’énergie gardent trace de cette histoire et de la diversité des manifestations matérielles de l’énergie.
En vue de passer en revue les principales unités employées pour cette grandeur qu’est l’énergie, il faut partir de ce qui nous est le plus sensible dans la vie courante : chaleur, alimentation, effort physique. Est ainsi introduite une deuxième grandeur importante, la puissance, qui exprime le flux d’énergie, c.à.d. une variation d’énergie par unité de temps. En seront alors déduits des exemples utilisant les unités et fournissant des ordres de grandeurs pour différentes activités comme l’alimentation, le sport, le chauffage, l’automobile, l’énergie solaire, une centrale thermique, le tout s’achevant par le bilan énergétique d’un pays.
2. La kilocalorie, unité de chaleur
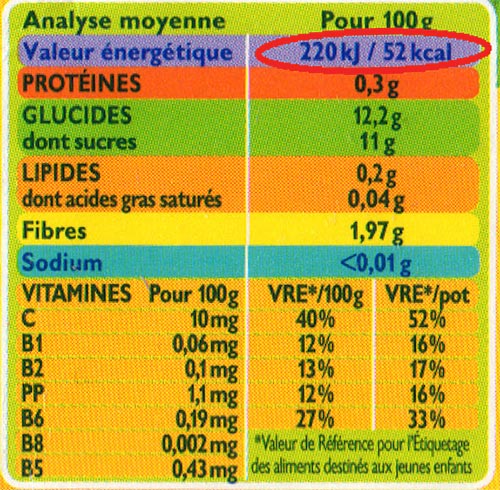
Tout emballage alimentaire comporte une description de la valeur nutritionnelle du produit, dont, en premier, son contenu énergétique exprimé en kilocalories, connu sous l’abréviation kcal (Figure 1).
Comme pour la masse[2] qui s’exprime en gramme, le multiple « kilo » de l’unité calories est retenu usuellement parce qu’il est le plus proche de nos possibilités corporelles (Figure 2). Une ration de céréales du matin apporte par exemple environ 150 kcal. Notre alimentation doit apporter chaque jour à un adulte, de 1800 à 2600 kcal, suivant le sexe, l’âge, la taille et l’activité physique.
La définition générique de la kilocalorie correspond à la quantité de chaleur qui élève d’un degré Celsius la température d’un kilogramme d’eau, par exemple de 14,5 à 15,5°C. Suivant cette définition, une ration alimentaire quotidienne de 2100 kcal élèverait de 35°C la température moyenne d’une masse d’eau de 60 kg. Cela illustre le fait que l’énergie apportée par l’alimentation permet de maintenir la chaleur corporelle, de faire fonctionner les organes et alimenter l’activité intellectuelle et musculaire. Ensuite, chauffer l’eau par un feu peut être réalisé avec des combustibles aux performances diverses. La combustion d’un kilogramme de bois, dégage environ 4300 kcal s’il est sec. La combustion d’un m3 de gaz, qui correspond à un volume d’un cube d’1 mètre de côté, apporte 9000 kcal et celle d’un kilogramme de fioul domestique 10.000 kcal.
L’instrument qui a permis de mesurer ces quantités d’énergies est le calorimètre, une enceinte qui ne laisse pas échapper la chaleur qu’elle contient, comme la bouteille thermos pour la boisson chaude (Figure 3). Le carburant brûle dans l’enceinte et chauffe une masse d’eau dans laquelle est plongé un thermomètre. La mesure des énergies de chaleur de combustion est alors permise grâce à la connaissance des masses de carburant et d’eau mises en jeu dans la réaction et la mesure de l’élévation de température due à la transformation.
3. Le kilowatt, unité de puissance du SI
Prenons une activité physique comme le vélo ou la marche. Qu’on accélère, ou qu’on monte une pente, on ressent bientôt une accélération des rythmes cardiaques et respiratoires en réponse à l’effort accompli. La lecture d’un compte-rendu d’étape du Tour de France, nous apprend que tel coureur a atteint une puissance de 300 à 400 watt dans la montée d’un col. Pour comparaison, une balade à vélo ou une randonnée en montagne, à rythme soutenu, requiert environ 100 watt.
La définition du kilowatt, ou millier de watts, est la puissance qui permet de déplacer, à la vitesse d’un mètre par seconde, le point d’application d’une force d’un kilonewton (kN), le kilonewton permettant de soulever une masse de 102 kg. Notée avec l’abréviation kW, le kilowatt correspond donc à la valeur de la puissance exercée pour élever une masse de 102 kilogrammes d’un mètre par seconde. Cette valeur est atteinte par un haltérophile sur les quelques secondes du lever de poids. Mais cette puissance est physiquement impossible à maintenir dans un sport d’endurance de longue durée comme la course de fond ou le cyclisme.
L’unité de puissance apparaît aussi pour mesurer la consommation électrique d’appareils ménagers. Un sèche-cheveu consomme un kilowatt (1 kW) à pleine puissance, un radiateur électrique deux à trois kilowatt. D’autres appareils électriques ont des puissances plus petites, exprimées en watts : une ampoule à incandescence consomme 75W et une ampoule à basse consommation 15W pour produire la même quantité de lumière. Une télévision consomme environ 250W, de même qu’un ordinateur portable. Un réfrigérateur consomme lui 100 W quand il se met en marche.
4. Energie versus puissance : grandeur de stock et grandeur de flux
Une grande différence existe donc entre les deux grandeurs décrites jusqu’à présent. Dans l’unité de chaleur, la kilocalorie, il n’y a aucune référence au temps. La chaleur est une grandeur statique traduisant le niveau d’un stock. Dans l’expérience de mesure du pouvoir calorifique d’un combustible, on mesure deux états de repos à l’intérieur du calorimètre : le premier avant la mise à feu du combustible, le deuxième suffisamment longtemps après la combustion pour que la température ait eu le temps de s’uniformiser. La chaleur de combustion est la différence entre ces deux états, indépendamment de la durée de la transition.
Au contraire, la définition de l’unité de puissance contient le temps. La puissance est une grandeur dynamique et représente un flux. C’est un flux d’énergie qui accompagne une transformation du système matériel, comme par exemple lors du lever de l’haltère. De même, une petite quantité de poudre fait beaucoup de bruit lors de l’explosion d’un pétard. Mais la même quantité de poudre ne fait aucun bruit lorsqu’elle se consume lentement. Dans le premier cas, le pétard explose car la durée de la transformation est très courte et la puissance est élevée. Dans le deuxième cas, la poudre se consume lentement et la puissance est faible. Toutefois, l’énergie de la combustion a été la même pour les deux expériences.
5. Le cheval-vapeur, autre unité de puissance
Cette unité de puissance n’est pas retenue dans le système international (SI) mais elle encore utilisée par les motoristes pour désigner la puissance maximale d’un moteur de voiture, de train, d’avion ou de bateau.
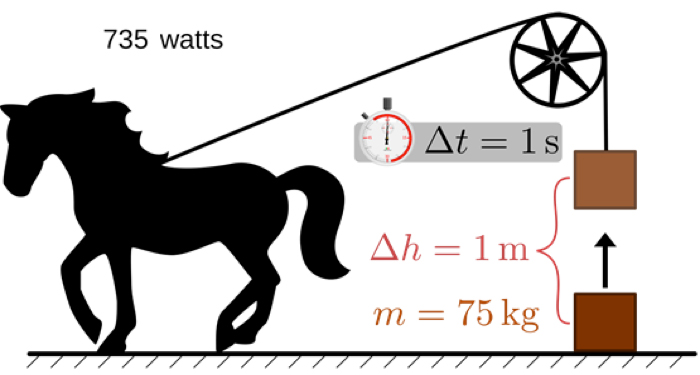
La définition du cheval-vapeur est la puissance développée pour élever une masse de 75 kg d’un mètre en une seconde[3] (Figure 4). Son abréviation est ch. Cette unité, choisie comme référence pour les machines à vapeur, est de l‘ordre de grandeur de l’effort que peut développer un cheval bien constitué. En comparaison de la puissance d’un kilowatt dépensée pour soulever 102 kg à la même vitesse d’un mètre seconde, le cheval-vapeur, soulevant une masse de 75kg représente une puissance de 735 W.
Voici quelques exemples de puissance de moteurs : pour une voiture moyenne, c’est 100 ch et six fois plus pour une voiture de F1. Pour un TGV entre 9000 et 12 000 ch suivant le modèle. Mais l’usage du cheval-vapeur disparaît peu à peu dans ce secteur laissant le kilowatt comme seule unité de puissance. Cette simplification va dans le bon sens, à condition de garder présent à l’esprit l’ordre de grandeur que le kilowatt représente car le cheval-vapeur évoque bien un ordre de grandeur.
6. Le kilojoule, unité de travail
Le travail est une grandeur statique comme la chaleur. Mais elle s’en distingue par son effet mécanique, comme l’ascension réalisée par le cycliste. Le travail est alors défini comme le produit de l’action d’une puissance mécanique sur une durée donnée. Dans une définition équivalente, c’est le produit du déplacement d’une force sur une distance donnée.
Comme pour la définition du kilowatt, un kilojoule est le travail exercé pour déplacer une force d’un kilonewton sur une distance d’un mètre, par exemple, élever d’un mètre une masse de 102 kg. Le kilojoule correspond donc au gain d’énergie obtenu par l’action d’une puissance d’un kilowatt pendant une seconde.
Le développement d’une puissance d’un kilowatt (ou, ce qui revient au même, la levée d’une masse de 102 kg) dépasse les possibilités humaines, sauf celles de l’haltérophile. Mais le commun des mortels peut déployer une puissance de cent watts pendant dix secondes (ou élever 10,2 kg de 10 m), réalisant ainsi le même travail d’un kilojoule. Les machines mécaniques simples, leviers ou cabestans, fonctionnent sur ce principe qui met à la portée de la puissance humaine l’accomplissement d’un travail donné en réduisant la puissance nécessaire. En contrepartie, la durée de l’effort est augmentée en proportion inverse, car il faut dans tous les cas réaliser le travail qui est le produit de la puissance sur la durée.
7. Le kilowattheure, unité d’énergie pratique
C’est une autre unité d’énergie construite à partir de l’unité de puissance, le watt. Elle est très pratique à condition de bien garder présent à l’esprit la distinction entre puissance qui est un flux et énergie qui est la variation d’un stock par l’action du flux sur une durée donnée. L’unité de temps du système international étant la seconde, le joule est l’énergie, ou variation du stock, produite sur la durée d’une seconde par une puissance, ou flux, d’un watt.
Le wattheure est la même notion étendue à une durée d’une heure ; c’est l’énergie, ou variation du stock, produite pendant une heure par une puissance, ou flux, d’un watt. Cette unité est plus pratique car l’heure est plus proche des durées de la vie courante que la seconde, trop petite. L’heure comptant 3 600 secondes, le wattheure vaut 3 600 joules ou 3,6 kilojoules. Quant au kilowattheure indiqué sur les relevés d’électricité ou de gaz, il vaut mille fois plus soit 3,6 mégajoules.
8. Le kilojoule, unité d’énergie du système international de référence
Jusqu’au milieu du 19ème siècle, chaleur et travail étaient deux concepts séparés. Toutefois, on avait observé que de la chaleur pouvait résulter du freinage d’un mouvement et une théorie identifiait la chaleur à une forme de mouvement microscopique[4]. Joule, un physicien anglais, réalisa la démonstration expérimentale de cette théorie en freinant un mouvement au point de presque l’immobiliser, et en mesurant la chaleur produite dans un calorimètre[5]. Ce mouvement était la rotation d’un arbre muni de pales, le tout immergé dans un liquide très visqueux qui freine le mouvement.
Supposons que le rotor est entraîné par un câble auquel est suspendue une masse de 102 kg. La descente de cette masse d’un mètre produit un travail d’un kilojoule. La descente est très lente à cause du freinage ; tout le travail est utilisé à vaincre la résistance que le liquide visqueux oppose au mouvement des pales. Dans un calorimètre dont la capacité thermique équivaut à un kilogramme d’eau, on mesure une élévation de température de 0,24°C, indiquant une création de chaleur de 240 calories.
Joule a montré la constance de cette création de chaleur par destruction de travail ;—240 calories créées pour un kilojoule de travail détruit — en multipliant les expérimentations : diverses destructions de travail dans des fluides visqueux, « freinage » d’un courant électrique dans une résistance chauffante. Cette invariance du rapport de la chaleur produite par destruction de travail est le premier principe de la thermodynamique. Et le joule s’est imposé comme unité d’énergie, quelle que soit sa nature mécanique, électrique ou calorique.
9. Distinction nécessaire entre énergie thermique, mécanique ou électrique
Le joule a ainsi supplanté la calorie dans la mesure de l’énergie, quelle que soit sa forme : mécanique, électrique ou calorique. Même dans l’alimentation où la calorie (ou plutôt la kilocalorie) est restée en usage, on voit qu’elle est accompagnée de sa conversion en kilojoule sur les étiquettes alimentaires. Cette simplification dans les unités peut faire penser que les formes calorique et mécanique de l’énergie sont équivalentes. C’est faux car l’expérience de Joule ne concerne que la destruction de travail produisant de la chaleur ; là seulement tout le travail est converti en chaleur.
En revanche, lors de la transformation inverse, de la chaleur en travail, telle que produite dans un moteur thermique, on ne peut jamais convertir la totalité de la chaleur en travail. Seule une partie de la chaleur peut l’être et le reste est rejeté dans l’environnement. C’est la condition nécessaire de la transformation de chaleur en travail exprimée dans le second principe de la thermodynamique découvert par Carnot (Lire : La thermodynamique : les lois. et La thermodynamique : énergie et entropie).
Dans les centrales thermiques[6] qui fournissent une grande partie de notre électricité, la chaleur est la forme initiale de l’énergie. Elle est convertie en action mécanique dans la turbine, puis électrique dans l’alternateur. L’énergie électrique produite n’est qu’une partie de l’énergie thermique consommée, d’après le principe de Carnot[7]. Aussi faut-il distinguer l’énergie thermique entrante et l’énergie électrique produite. Pour cela, on utilise des suffixes : kWhth (pour thermique) et kWhe (pour électrique). Il en est de même pour les puissances : Wth pour la puissance thermique et We pour la puissance électrique. Ainsi une centrale thermique ayant une capacité de production électrique de 1000 MWe consomme une puissance thermique de 3000 MWth dans la chaudière. La différence, 2000 MW, est la chaleur absorbée par le condenseur puis rejetée dans l’environnement. Une partie peut alors être utilisée dans le chauffage de locaux, quand le procédé est rentable.
10. La tonne-équivalent pétrole (tep)
C’est l’unité retenue actuellement dans les études économiques et pour les bilans énergétiques annuels des différents pays, de l’Union européenne (UE) ou du monde. Il y a quelques décennies, lorsque le charbon minéral était la principale source d’énergie consommée dans le monde, la référence était la tonne équivalent charbon (tec). La tep mesure la chaleur produite par la combustion d’une tonne de pétrole[8]. La valeur standard est 41,9 GJ (gigajoules) ou 11,6 MWh (mégawattheures).
L’utilisation de la tep dans les bilans énergétiques complique plus qu’elle ne simplifie l’exposé des questions énergétiques. En effet, les mêmes bilans utilisent le MWh pour chiffrer la production électrique et le GJ pour quantifier la production de chaleur. Or, comment peut-on apprécier les ordres de grandeur et les rapports entre les différentes formes d’énergie quand leurs valeurs sont exprimées dans plusieurs unités ? Aussi difficilement que quand les prix de produits sont exprimés dans des monnaies différentes. La tep peut difficilement jouer ce rôle d’unité universelle car elle ne résistera pas à la fin de la domination du pétrole. N’est-il pas paradoxal de parler de la fin prochaine du pétrole tout en continuant d’utiliser la tep dans les bilans énergétiques nationaux ou internationaux ? Sans parler de la curiosité que représente la mesure d’une production éolienne en tep.
Conclusion : pour une unité plus compréhensible dans les bilans annuels
Tout abonné du réseau électrique reçoit des relevés de consommation en kWh. Il en est de même pour le gaz ou la chaleur. Dans un souci de compréhension du public, il serait donc préférable d’utiliser le kWh ou ses multiples pour unifier les bilans de toutes les sources d’énergie. Ce serait déjà un grand pas d’accompli.
Les bilans annuels pourraient aussi être établis en kilowattans (kWa). La définition en est simple : alors que le kWh est la quantité d’énergie consommée pour délivrer une puissance d’un kW pendant une heure, le kWa est la quantité d’énergie consommée pour délivrer cette même puissance pendant une année de 365 jours, soit 8 760 heures. Un kWa vaut donc 8 760 kWh.
Les bilans énergétiques de pays, de sous-continents ou continents, comme l’Union européenne, l’Afrique, ou le monde sont toujours donnés pour une année et regroupent toutes les sources d’énergie. Le plus clair et le plus simple serait donc de les exprimer dans une unité qui soit :
– indépendante de toute énergie particulière (comme le kWh ou kWa)
– consistante avec la durée de la mesure, l’année, ce qui est le cas du kWa.
La référence à l’année pour mesurer l’énergie dans ce contexte des bilans énergétiques a par ailleurs l’avantage de fournir une comparaison immédiate entre la production d’énergie et les puissances installées de production des centrales hydroélectriques, thermiques conventionnelles ou nucléaires ainsi que des fermes solaires ou éoliennes.
Notes et références
[1] Le nom de Système international d’unités, reconnu également sous l’abréviation SI, a été officiellement adopté par la Conférence générale des poids et mesures lors de sa 11e réunion en 1960. Il consiste en un ensemble de 7 unités de base : le mètre (distance), le kilogramme (masse), la seconde (temps), l’ampère (intensité électrique), le kelvin (température), la mole (quantité de matière) et la candela (intensité lumineuse). A cela s’ajoute des préfixes et d’unités dérivées. Voir Bureau International des Poids et mesures.
[2] La masse est une propriété physique fondamentale d’un corps et traduit la quantité de matière contenue dans celui-ci. Voir Futura Sciences.
[3] Il ne faut pas le confondre avec le cheval fiscal (CV) dans le cas des voitures qui dépend de la valeur normalisée d’émission de dioxyde de carbone (CO2) en grammes par kilomètre (g/km) et de la puissance maximale du moteur (en kilowatts ou cheval-vapeur).
[4] Soit la théorie du transfert thermique qui correspond à un transfert d’énergie microscopique produisant de la chaleur
[5] James Joule (1818-1889) a étudié la nature de la chaleur et découvert sa relation avec le travail mécanique, ce qui a conduit à la théorie de la conservation de l’énergie, première loi de la thermodynamique. Il a également énoncé une relation entre le courant électrique traversant une résistance et la chaleur dissipée par celle-ci, appelée au 20ème siècle la loi de Joule U=RI. Enfin il a travaillé avec Lord Kelvin pour développer l’échelle absolue de température et a étudié la magnétostriction. Dans le Système international, l’unité de l’énergie et de la quantité de chaleur porte son nom : le joule.
[6] Centrales thermiques partant toutes d’une source de chaleur alimentant un cycle thermodynamique : chaleur de combustion du gaz, du fioul-oil ou de la biomasse,dans les centrales conventionnelles, chaleur de fission de l’uranium dans les centrales nucléaires, chaleur solaire concentrée dans les centrales solaires thermodynamiques ou chaleur de la croûte terrestre dans les centrales géothermiques.
[7] Le scientifique français Sidi Carnot a publié en 1824 un ouvrage scientifique sur les machines thermiques et démontré qu’il est impossible d’obtenir un rendement maximal de 100% pour les machines thermiques.
[8] Cette mesure a été standardisée car il y a des variations du contenu énergétique de la ressource suivant l’origine du pétrole
L’Encyclopédie de l’Énergie est publiée par l’Association des Encyclopédies de l’Environnement et de l’Énergie (www.a3e.fr), contractuellement liée à l’université Grenoble Alpes et à Grenoble INP, et parrainée par l’Académie des sciences.
Pour citer cet article, merci de mentionner le nom de l’auteur, le titre de l’article et son URL sur le site de l’Encyclopédie de l’Énergie.
Les articles de l’Encyclopédie de l’Énergie sont mis à disposition selon les termes de la licence Creative Commons Attribution – Pas d’Utilisation Commerciale – Pas de Modification 4.0 International.